חום כמוס ושינויי מצב צבירה
כשמוסיפים חום - אבל הטמפרטורה לא עולה
 תופעה מפתיעה
תופעה מפתיעה
 מהו חום כמוס?
מהו חום כמוס?
 חום כמוס - הגדרה
חום כמוס - הגדרה
חום כמוס הוא כמות האנרגיה הנדרשת לשנות את מצב הצבירה של 1 ק"ג חומר, ללא שינוי בטמפרטורה.
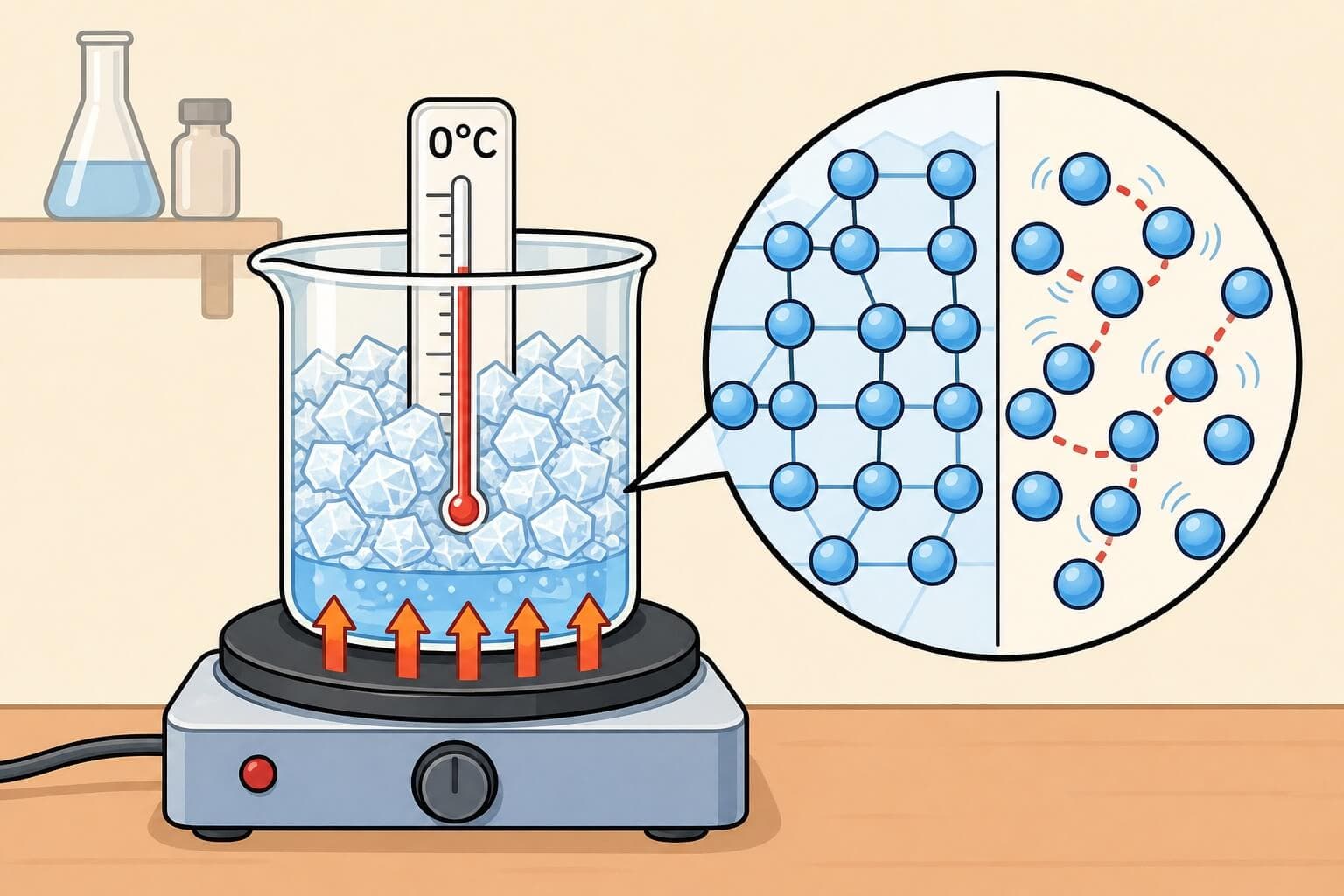
בזמן שינוי מצב צבירה, כל האנרגיה שנספגת משמשת לשבירת קשרים בין חלקיקים, ולא להגברת התנועה שלהם.
כיוון שטמפרטורה מודדת ממוצע אנרגיה קינטית (מהירות תנועה), והאנרגיה הולכת לשבירת קשרים (לא לתנועה) - הטמפרטורה לא משתנה.
שני סוגי חום כמוס:
- חום כמוס של היתוך (Lf): מוצק ← נוזל
- חום כמוס של רתיחה (Lv): נוזל ← גז
היחידה: ג'ול לקילוגרם (J/kg)
בזמן שינוי מצב, טמפרטורה קבועה - כי האנרגיה הולכת לשבירת/יצירת קשרים, לא להגברת תנועה.
 הנוסחה
הנוסחה
Q = m x L
Q = כמות חום (ג'ול)
m = מסה (ק"ג)
L = חום כמוס (J/kg)
למים:
- חום כמוס של היתוך: Lf = 334,000 J/kg
- חום כמוס של רתיחה: Lv = 2,260,000 J/kg
שימו לב: חום כמוס של רתיחה גדול פי 7 מחום כמוס של היתוך - כי בגז הקשרים בין חלקיקים נשברים לחלוטין.
 עקומת החימום של מים
עקומת החימום של מים
אם מחממים קרח מ-20- מעלות ועד שהמים מתאדים, מקבלים עקומת חימום עם חמישה שלבים. זהו גרף טמפרטורה כפונקציה של זמן (או של חום שנוסף):
1. קרח מתחמם
מ-20- ל-0 מעלות.
טמפרטורה עולה.
נוסחה: Q = mc(קרח)DeltaT
2. היתוך
0 מעלות.
קרח ← מים.
טמפרטורה קבועה.
Q = m x Lf
3. מים מתחממים
מ-0 ל-100 מעלות.
טמפרטורה עולה.
Q = mc(מים)DeltaT
4. רתיחה
100 מעלות.
מים ← קיטור.
טמפרטורה קבועה.
Q = m x Lv
5. קיטור מתחמם
מעל 100 מעלות.
טמפרטורה עולה שוב.
Q = mc(קיטור)DeltaT
 שינויי מצב צבירה - סיכום
שינויי מצב צבירה - סיכום
שינויי מצב צבירה
| שינוי | כיוון | אנרגיה | קשרים | שם התהליך |
|---|---|---|---|---|
| היתוך | מוצק ← נוזל | קולטת חום | שוברת קשרים | המסה |
| קיפאון | נוזל ← מוצק | פולטת חום | יוצרת קשרים | הקפאה |
| רתיחה/אידוי | נוזל ← גז | קולטת חום | שוברת קשרים | התאדות |
| עיבוי | גז ← נוזל | פולטת חום | יוצרת קשרים | התעבות |
| הפשרה | מוצק ← גז | קולטת חום | שוברת קשרים | סובלימציה |
* שבירת קשרים = קליטת אנרגיה. יצירת קשרים = פליטת אנרגיה. זה אותו עיקרון כמו בקשרים כימיים!
 הבדל קריטי: אידוי מול רתיחה
הבדל קריטי: אידוי מול רתיחה
 אידוי מול רתיחה
אידוי מול רתיחה
 אידוי
אידוי
מתרחש בכל טמפרטורה.
רק מפני השטח של הנוזל.
תהליך איטי.
חלקיקים מהירים במיוחד 'בורחים' מפני השטח.
דוגמה: ייבוש כביסה, התאדות שלולית, הזעה
 רתיחה
רתיחה
מתרחשת רק בטמפרטורת הרתיחה.
בכל הנפח של הנוזל.
תהליך מהיר ואינטנסיבי.
בועות גז נוצרות בתוך הנוזל.
דוגמה: מים רותחים בקומקום, חלב שגולש
אידוי הוא הסיבה שכביסה מתייבשת גם בחורף - לא צריך הגיע ל-100 מעלות
 דוגמאות מפתיעות מהחיים
דוגמאות מפתיעות מהחיים
 חום כמוס בפעולה
חום כמוס בפעולה
הזעה מקררת
כשזיעה מתאדית מהעור, היא קולטת חום כמוס מהגוף ומקררת אותו. לכן מרגישים קר אחרי מקלחת - המים מתאדים וקולטים חום מהעור.
קרח במשקה
קרח מקרר משקה הרבה יותר ממים קרים באותה טמפרטורה. כי בנוסף לקליטת חום, הקרח צריך חום כמוס כדי להימס - והוא 'גונב' חום מהמשקה.
סובלימציה
קרח יבש (CO2 מוצק) עובר ישירות ממוצק לגז - בלי שלב נוזלי. גם שלג יכול להיעלם בלי להימס (סובלימציה) בתנאים של אוויר יבש וקר.
מזגן
מזגן עובד על אידוי נוזל קירור בתוך הבית (קולט חום - מקרר) ועיבוי שלו מחוץ לבית (פולט חום). לכן המזגן פולט אוויר חם החוצה.
 חישוב כולל - עקומת חימום
חישוב כולל - עקומת חימום
 דוגמת חישוב מלא
דוגמת חישוב מלא
שאלה: כמה אנרגיה נדרשת לחמם 500g קרח מ-10- מעלות עד מים ב-50 מעלות?
שלב 1: חימום קרח מ-10- ל-0
Q1 = 500 x 2.1 x 10 = 10,500 J
(חום סגולי קרח = 2.1 J/(g x C))
שלב 2: היתוך קרח למים ב-0 מעלות
Q2 = 500 x 334 = 167,000 J
(חום כמוס היתוך = 334 J/g)
שלב 3: חימום מים מ-0 ל-50
Q3 = 500 x 4.2 x 50 = 105,000 J
סה"כ: Q = 10,500 + 167,000 + 105,000 = 282,500 J
שימו לב: שלב ההיתוך לבד דורש יותר אנרגיה מחימום המים ב-50 מעלות!
 שאלה לחשיבה
שאלה לחשיבה
מדוע כוויה מקיטור ב-100 מעלות חמורה יותר מכוויה ממים רותחים ב-100 מעלות?
למרות שהטמפרטורה זהה (100 מעלות), הקיטור מכיל אנרגיה נוספת - החום הכמוס של הרתיחה. כשהקיטור נוגע בעור, הוא עובר עיבוי (גז ← נוזל) ופולט את כל החום הכמוס הזה לעור, בנוסף לחום הרגיל. חום כמוס רתיחה של מים = 2,260 J/g - זו כמות אנרגיה עצומה.
 שאלה לחשיבה
שאלה לחשיבה
מדוע מרגישים קר כשיוצאים מהבריכה גם כשחם בחוץ?
כשיוצאים מהבריכה, טיפות מים על העור מתחילות להתאדות. אידוי הוא תהליך קולט חום - המים 'גונבים' חום מהעור כדי לשבור את הקשרים בין חלקיקיהם. לכן העור מתקרר ומרגישים צמרמורת. רוח מחזקת את האידוי ואת תחושת הקור.
 שאלה לחשיבה
שאלה לחשיבה
למה בעקומת החימום, קטע הרתיחה (שלב 4) ארוך בהרבה מקטע ההיתוך (שלב 2)?
כי החום הכמוס של רתיחה (2,260 J/g) גדול פי 7 מהחום הכמוס של היתוך (334 J/g). במעבר מנוזל לגז צריך לנתק את החלקיקים לחלוטין זה מזה, בעוד שבהיתוך רק מרפים את הסדר הקשיח. לכן דרוש הרבה יותר אנרגיה לרתיחה.
כשמרססים חנקן נוזלי (-196 מעלות) על מזון, ההקפאה היא כמעט מיידית. החנקן הנוזלי רותח (הופך לגז) וסופג כמות עצומה של חום כמוס מהמזון. התהליך כל כך מהיר שגבישי הקרח שנוצרים הם זעירים - וזה שומר על איכות המזון. לכן גלידה שמוכנת עם חנקן נוזלי היא חלקה במיוחד - אין בה גבישי קרח גדולים.
 חום כמוס של חומרים שונים
חום כמוס של חומרים שונים
חום כמוס של היתוך ורתיחה
| חומר | נקודת היתוך (C) | Lf (J/g) | נקודת רתיחה (C) | Lv (J/g) |
|---|---|---|---|---|
| מים | 0 | 334 | 100 | 2,260 |
| אלכוהול (אתנול) | -114 | 108 | 78 | 846 |
| ברזל | 1,538 | 247 | 2,862 | 6,090 |
| אלומיניום | 660 | 397 | 2,519 | 10,900 |
| חנקן | -210 | 25.5 | -196 | 199 |
* שימו לב: לחומרים שונים יש חום כמוס שונה. חום כמוס הרתיחה תמיד גבוה מחום כמוס ההיתוך
 נקודות מפתח לזכור
נקודות מפתח לזכור
סיכום חום כמוס:
- בשינוי מצב צבירה - טמפרטורה קבועה, כי האנרגיה הולכת לקשרים
- Q = m x L (חום = מסה x חום כמוס)
- חום כמוס רתיחה > חום כמוס היתוך (פי 7 במים)
- אידוי = בכל טמפרטורה, מפני השטח. רתיחה = רק בטמפרטורת רתיחה, בכל הנפח
- עיבוי (גז ← נוזל) פולט חום - לכן כוויית קיטור חמורה