ריבוזום והרכבת חלבונים
מפעל הייצור של התא
 מ-DNA לחלבון - זרימת המידע בתא
מ-DNA לחלבון - זרימת המידע בתא
 הדוגמה המרכזית של הביולוגיה
הדוגמה המרכזית של הביולוגיה
ה-DNA מכיל את ההוראות לבניית חלבונים. הריבוזום הוא המכונה שקוראת את ההוראות ובונה את החלבונים.
התהליך מתרחש בשלושה שלבים:
שלב 1 - DNA (בגרעין):
ה-DNA מכיל את ה'מתכון' - רצף הבסיסים שמקודד את סדר חומצות האמינו בחלבון.
שלב 2 - תעתוק (בגרעין):
המידע מועתק מ-DNA לRNA שליח (mRNA) - מולקולה שיכולה לצאת מהגרעין ולנסוע לריבוזום.
שלב 3 - תרגום (בריבוזום):
הריבוזום קורא את ה-mRNA ומרכיב חומצות אמינו בסדר הנכון ← נוצר חלבון.
DNA ← RNA ← חלבון ← תכונה. זהו 'הדוגמה המרכזית' של הביולוגיה המולקולרית.
 שלבי הרכבת חלבון
שלבי הרכבת חלבון
 מ-DNA לחלבון - שלב אחר שלב
מ-DNA לחלבון - שלב אחר שלב
תעתוק
בגרעין
ה-DNA 'נפתח' באזור הגן הנדרש
נבנה עותק mRNA של הגן
ה-mRNA יוצא מהגרעין דרך נקבוביות
ה-DNA נשאר מוגן בגרעין
תרגום
בריבוזום (ציטופלזמה)
ה-mRNA מתחבר לריבוזום
הריבוזום קורא קודונים (שלשות בסיסים)
כל קודון מקודד לחומצת אמינו ספציפית
חומצות אמינו מתחברות בשרשרת ← חלבון
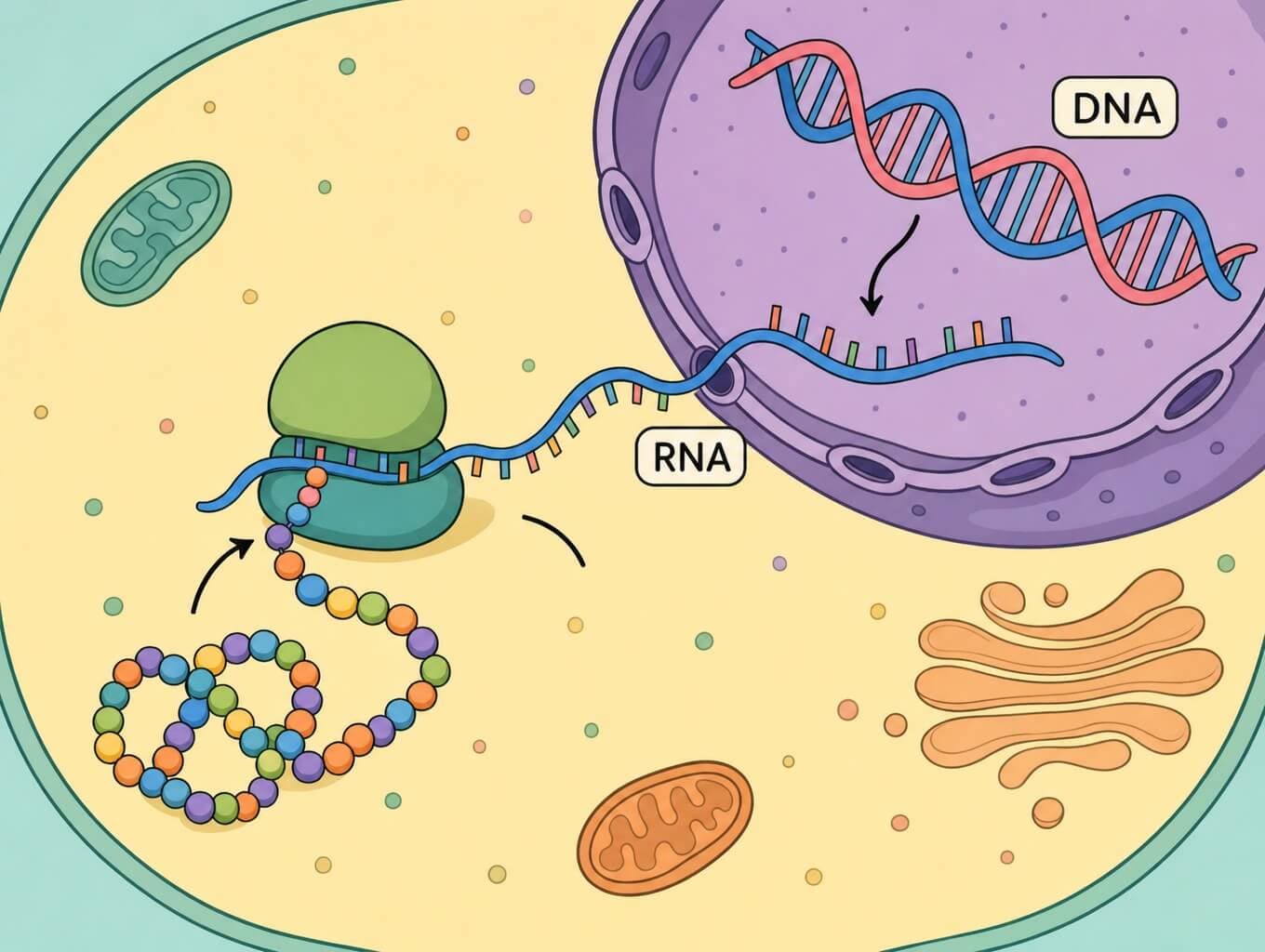
אנלוגיה: ה-DNA הוא כמו ספר מתכונים שנשמר בספרייה (גרעין). ה-mRNA הוא כמו צילום של מתכון אחד שנלקח למטבח. הריבוזום הוא השף שקורא את המתכון ומרכיב את המנה (חלבון).
 הריבוזום
הריבוזום
מבנה ומיקום הריבוזום
הריבוזום הוא אברון קטן שבנוי מRNA ריבוזומלי (rRNA) וחלבונים.
הוא לא מוקף בקרום.
ממוקם בציטופלזמה - חופשי או על הרשת האנדופלזמית המחוספסת.
כל תא מכיל אלפי ריבוזומים - כי הוא צריך לייצר חלבונים כל הזמן.
 מ-DNA לתכונה
מ-DNA לתכונה
המסלול השלם הוא: DNA ← RNA ← חלבון ← תכונה. לדוגמה:
 דוגמאות: מגן לתכונה
דוגמאות: מגן לתכונה
צבע עיניים
גן ב-DNA ← mRNA ← חלבון שמייצר פיגמנט מלנין ← עיניים חומות (או חוסר פיגמנט ← עיניים כחולות)
סוג דם
גן ב-DNA ← mRNA ← חלבון על פני תאי דם אדומים ← סוג דם A, B, AB או O
מחלת מגל
שינוי בבסיס אחד ב-DNA ← חלבון המוגלובין שונה ← תאי דם בצורת מגל ← מחלה
עמידות לאנטיביוטיקה
מוטציה ב-DNA של חיידק ← חלבון שונה ← החיידק עמיד לתרופה
 שאלה לחשיבה
שאלה לחשיבה
ה-DNA נמצא בגרעין אבל הריבוזומים בציטופלזמה. למה לא 'לייצר' חלבונים ישירות מה-DNA?
ה-DNA חשוב מדי כדי 'להוציא' אותו מהגרעין - יש רק עותק אחד (שניים, בגרעין דיפלואידי) של כל גן. יציאה מהגרעין עלולה לחשוף אותו לנזק. במקום זה, נוצר 'עותק זמני' (mRNA) שנשלח לציטופלזמה. ניתן ליצור הרבה עותקי mRNA מגן אחד - ולייצר הרבה חלבונים במקביל.
 שאלה לחשיבה
שאלה לחשיבה
אם כל תא בגוף מכיל את אותו DNA, למה תא שריר מייצר חלבונים שונים מתא עצב?
למרות שה-DNA זהה בכל התאים, כל סוג תא מפעיל (מתעתק) רק את הגנים הרלוונטיים לתפקידו. תא שריר מתעתק גנים של אקטין ומיוזין (חלבוני שריר), ותא עצב מתעתק גנים של חלבוני עצב. שאר הגנים 'מושתקים'. זה נקרא ביטוי גנים דיפרנציאלי.
 למה כל כך הרבה ריבוזומים?
למה כל כך הרבה ריבוזומים?
תא ממוצע מכיל כ10 מיליון ריבוזומים! תא כבד, שמייצר כמויות עצומות של חלבונים, עשוי להכיל אפילו יותר. למה? כי התא צריך לייצר אלפי סוגי חלבונים שונים בו-זמנית - אנזימים, חלבוני מבנה, חלבוני הובלה, נוגדנים ועוד. ריבוזומים רבים עובדים על אותו mRNA במקביל (נקרא פוליזום) כדי לייצר עותקים רבים של אותו חלבון במהירות.
 חלבונים - הצבא שמנהל את התא
חלבונים - הצבא שמנהל את התא
אנזימים (זרזים)
מזרזים תגובות כימיות.
דוגמה: עמילאז, פפסין, קטלאז.
ללא אנזימים, התגובות היו איטיות מדי.
חלבוני מבנה
בונים את שלד התא.
דוגמה: קולגן (בעור), קרטין (בשיער).
נותנים לתאים ולרקמות את צורתם.
חלבוני הובלה
מובילים חומרים.
דוגמה: המוגלובין (מוביל חמצן בדם).
חלבוני הקרום מובילים חומרים דרך הממברנה.
חלבוני הגנה
מגנים על הגוף.
דוגמה: נוגדנים (מערכת החיסון).
מזהים ומנטרלים פולשים (חיידקים, וירוסים).
לפעמים מתרחשת טעות בהעתקת ה-DNA או בתעתוק ל-RNA. שינוי כזה נקרא מוטציה.
אם מוטציה מתרחשת בגן, הקודונים ב-mRNA משתנים ← חומצת אמינו שונה עלולה להיכנס לחלבון ← החלבון עלול לשנות צורה ותפקוד.
לא כל מוטציה גורמת לשינוי. לפעמים השינוי לא משנה את חומצת האמינו (בגלל ריבוי הקוד הגנטי), ולפעמים השינוי בחומצת אמינו לא משפיע על צורת החלבון.
מוטציות יכולות להיות: מזיקות (מחלות גנטיות), ניטרליות (ללא השפעה), או לעיתים נדירות - מועילות (בסיס לאבולוציה).
הבנת זרימת המידע DNA ← RNA ← חלבון פתחה את הדרך להנדסה גנטית. מדענים יכולים להכניס גן מאורגניזם אחד לאורגניזם אחר - וה'שפה' אוניברסלית, אז הריבוזומים של הנמען יקראו את ה-mRNA ויייצרו את החלבון הרצוי.
דוגמה: אינסולין לחולי סוכרת. בעבר הפיקו אינסולין מלבלב של חזירים ובקר. היום, הגן האנושי לאינסולין מוכנס לחיידק E. coli, והחיידק מייצר אינסולין אנושי מושלם. חולי סוכרת ברחבי העולם מזריקים לעצמם אינסולין שיוצר על ידי חיידקים.
CRISPR: טכנולוגיה חדשה (שזכתה בפרס נובל 2020) שמאפשרת 'לערוך' DNA בדיוק מדהים - כמו חיתוך והדבקה במעבד תמלילים. היא פותחת אפשרויות לריפוי מחלות גנטיות, אך מעלה גם שאלות אתיות עמוקות.