איזון משוואות כימיות
חוק שימור המסה ואיך ליישם אותו
 הרחבה
הרחבה
נושא זה הוא תוכן הרחבה (רשות). הוא מעמיק את ההבנה של תהליכים כימיים.
 חוק שימור המסה
חוק שימור המסה
חוק שימור המסה, שגילה אנטואן לבואזיה במאה ה-18, קובע שבתהליך כימי המסה הכוללת של המגיבים שווה למסה הכוללת של התוצרים.
חוק שימור המסה אומר: בתהליך כימי, אטומים לא נוצרים ולא נעלמים. הם רק מסתדרים מחדש.
משמעות: מספר האטומים מכל סוג חייב להיות זהה בצד המגיבים ובצד התוצרים.
לכן, כשכותבים משוואה כימית, צריך לאזן אותה - לוודא שכמות האטומים זהה בשני הצדדים.
איזון משוואה כימית הוא יישום ישיר של חוק שימור המסה.
אנלוגיה - לגו
דמיינו שיש לכם מבנה לגו עם 10 קוביות אדומות, 5 כחולות ו-3 צהובות. אתם מפרקים אותו ובונים מבנה חדש.
כמה קוביות יש לכם? עדיין 10 אדומות, 5 כחולות ו-3 צהובות! קוביות לא נעלמו ולא נוצרו - רק סידרתם אותן מחדש.
בדיוק כך עובדת תגובה כימית: האטומים הם 'הקוביות'. הם מסתדרים מחדש אבל לא נוצרים ולא נעלמים.
 איך מאזנים? - שלב אחר שלב
איך מאזנים? - שלב אחר שלב
 שלבי האיזון
שלבי האיזון
בצעו את השלבים הבאים לאיזון כל משוואה:
- כתבו את הנוסחאות של המגיבים והתוצרים (ללא שינוי)
- ספרו את מספר האטומים מכל סוג בשני הצדדים
- הוסיפו מקדמים (מספרים גדולים לפני הנוסחאות) עד שהכמויות משתוות
- בדקו שוב - כל סוג אטום חייב להיות זהה בשני הצדדים
 חוק ברזל
חוק ברזל
אסור לשנות את האינדקסים (המספרים הקטנים בתוך הנוסחה). שינוי אינדקס משנה את המולקולה עצמה! מותר רק להוסיף מקדמים (מספרים גדולים לפני הנוסחה).
לדוגמה: H2O ← H2O2 - זו לא אותה מולקולה! H2O = מים, H2O2 = מי חמצן.
 דוגמה מפורטת 1: יצירת מים
דוגמה מפורטת 1: יצירת מים
 איזון צעד אחר צעד
איזון צעד אחר צעד
דוגמה 1: יצירת מים
לא מאוזן: H2 + O2 ← H2O
ספירה: צד שמאל: 2H, 2O | צד ימין: 2H, 1O - חמצן לא מאוזן!
שלב 1: נכפיל את המים ב-2: H2 + O2 ← 2H2O
ספירה: צד שמאל: 2H, 2O | צד ימין: 4H, 2O - מימן לא מאוזן!
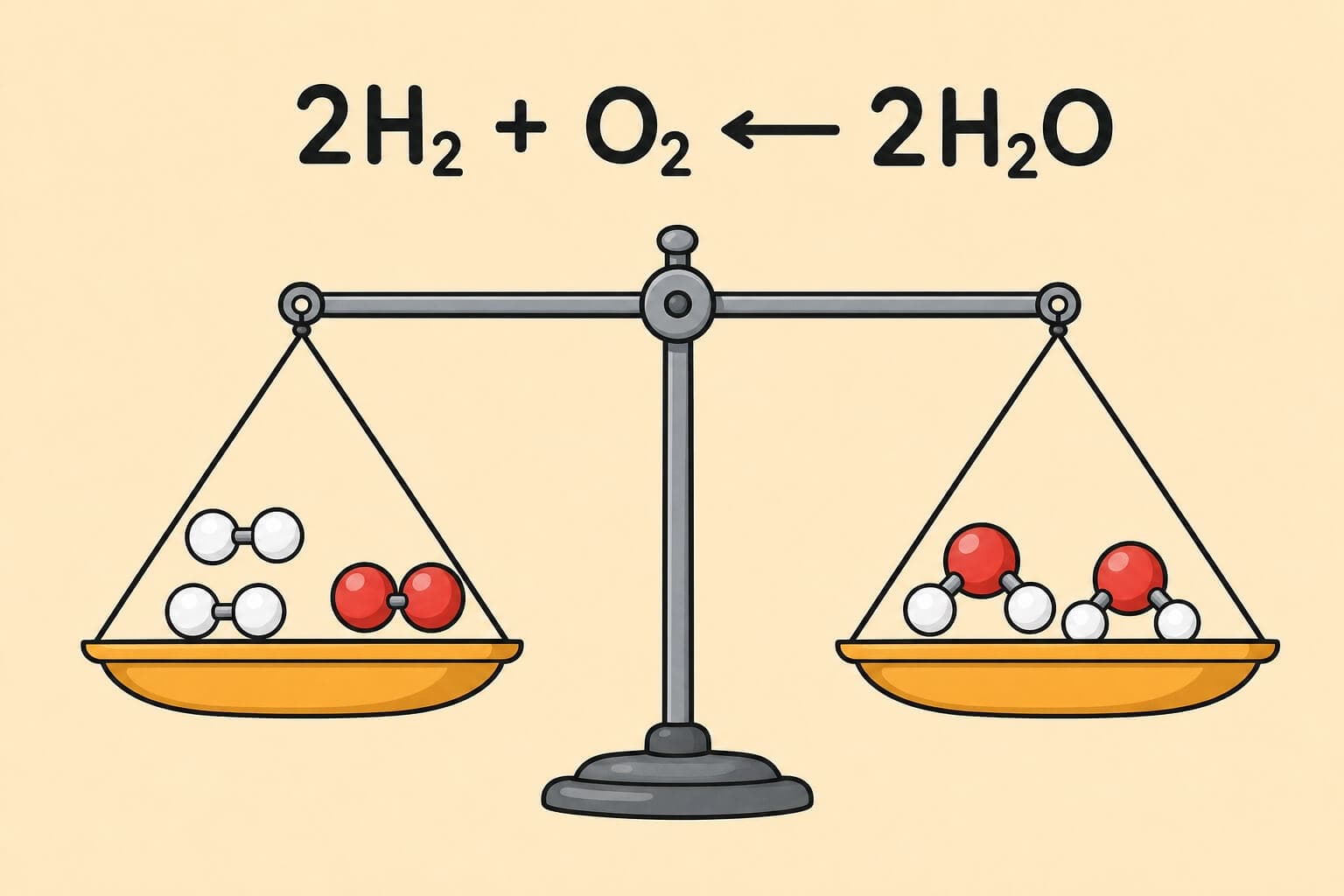
שלב 2: נכפיל את המימן ב-2: 2H2 + O2 ← 2H2O
ספירה: צד שמאל: 4H, 2O | צד ימין: 4H, 2O - מאוזן!
דוגמה 2: בעירת מתאן
לא מאוזן: CH4 + O2 ← CO2 + H2O
ספירה: צד שמאל: 1C, 4H, 2O | צד ימין: 1C, 2H, 3O
שלב 1: נאזן מימן: CH4 + O2 ← CO2 + 2H2O
ספירה: צד שמאל: 1C, 4H, 2O | צד ימין: 1C, 4H, 4O
שלב 2: נאזן חמצן: CH4 + 2O2 ← CO2 + 2H2O
ספירה: צד שמאל: 1C, 4H, 4O | צד ימין: 1C, 4H, 4O - מאוזן!
דוגמה 3: חלודה (ברזל + חמצן)
לא מאוזן: Fe + O2 ← Fe2O3
ספירה: צד שמאל: 1Fe, 2O | צד ימין: 2Fe, 3O - שניהם לא מאוזנים!
שלב 1: נכפיל Fe2O3 ב-2: Fe + O2 ← 2Fe2O3
צד ימין: 4Fe, 6O
שלב 2: נאזן ברזל: 4Fe + O2 ← 2Fe2O3
צד שמאל: 4Fe, 2O | צד ימין: 4Fe, 6O
שלב 3: נאזן חמצן: 4Fe + 3O2 ← 2Fe2O3
ספירה: 4Fe, 6O | 4Fe, 6O - מאוזן!
 טיפים לאיזון מהיר
טיפים לאיזון מהיר
הנה כמה טריקים שיעזרו לכם לאזן מהר יותר:
- התחילו מהיסוד שמופיע הכי פחות פעמים (בצד אחד בלבד)
- אזנו מתכות ואל-מתכות לפני חמצן ומימן
- השאירו את החמצן לסוף - הוא בדרך כלל מופיע בכמה מקומות
- אם קיבלתם שברים, כפלו את כל המקדמים במספר כדי לקבל מספרים שלמים
- תמיד בדקו את הכול בסוף!
 חוק שימור המסה בעולם האמיתי
חוק שימור המסה בעולם האמיתי
 למה זה חשוב?
למה זה חשוב?
חוק שימור המסה לא רק תיאוריה - הוא משמש בכל יום:
- תעשייה כימית - מפעלים צריכים לדעת בדיוק כמה מגיבים לקחת כדי לייצר כמות מסוימת של תוצר
- בישול - כשאופים עוגה, המסה הכוללת של המרכיבים (קמח + ביצים + סוכר) שווה למסת העוגה (פחות האדים שהתאדו)
- רפואה - חישוב מנות תרופות מבוסס על חישובים כימיים מדויקים
- סביבה - חישוב פליטות CO2 מבעירת דלקים מבוסס על איזון משוואות
 סימולציה - איזון משוואות כימיות
סימולציה - איזון משוואות כימיות
תרגלו איזון משוואות כימיות בעזרת הסימולציה האינטראקטיבית. הוסיפו מקדמים ובדקו אם המשוואה מאוזנת.
 סימולציה - חוק שימור המסה
סימולציה - חוק שימור המסה
בסימולציה הבאה תוכלו לראות בפועל שהמסה נשמרת בתהליך כימי - אטומים לא נוצרים ולא נעלמים, הם רק מסתדרים מחדש.
 שאלה לחשיבה
שאלה לחשיבה
אזנו את המשוואה: Fe + O2 ← Fe2O3
המשוואה המאוזנת: 4Fe + 3O2 ← 2Fe2O3
בדיקה: צד שמאל - 4 Fe, 6 O. צד ימין - 4 Fe (2 כפול 2), 6 O (2 כפול 3). מאוזן!
 שאלה לחשיבה
שאלה לחשיבה
אזנו את המשוואה: C3H8 + O2 ← CO2 + H2O (בעירת פרופאן - הגז בבלון ביתי)
C3H8 + 5O2 ← 3CO2 + 4H2O
בדיקה: צד שמאל - 3C, 8H, 10O. צד ימין - 3C (מ-3CO2), 8H (מ-4H2O), 10O (6 מ-3CO2 + 4 מ-4H2O). מאוזן! זו התגובה שמתרחשת כשמבשלים עם גז בבלון.
 שאלה לחשיבה
שאלה לחשיבה
שורפים נר במיכל סגור. מה יקרה למסה הכוללת בתוך המיכל? מדוע?
המסה הכוללת לא תשתנה. לפי חוק שימור המסה, אטומים לא נוצרים ולא נעלמים. השעווה והחמצן (מגיבים) הופכים ל-CO2 ומים (תוצרים), אבל כל האטומים נשארים בתוך המיכל. הנר ייכבה כשייגמר החמצן במיכל.
אנטואן-לוראן לבואזיה (1743-1794) היה כימאי צרפתי שניסח את חוק שימור המסה. הוא הראה באמצעות ניסויים מדויקים שבתגובה כימית, המסה הכוללת לא משתנה - אטומים רק מסתדרים מחדש.
לבואזיה גם גילה את תפקיד החמצן בבעירה (ובכך הפריך את 'תיאוריית הפלוגיסטון'), ופיתח את שיטת השמות הכימית שאנחנו משתמשים בה עד היום.
עובדה עצובה: לבואזיה הוצא להורג בגיליוטינה בזמן המהפכה הצרפתית בגיל 50 בלבד. המתמטיקאי לגראנז' אמר: 'נדרשה רק שנייה לחתוך את ראשו, ומאה שנה לא יספיקו ליצור ראש כזה.'
 מה הלאה?
מה הלאה?
בשיעורים הבאים נלמד על אנרגיה בתהליכים כימיים - מדוע חלק מהתגובות משחררות חום (כמו בעירה) וחלק דווקא קולטות חום (כמו פוטוסינתזה).