הקשר השיתופי (קוולנטי)
כאשר אטומים משתפים אלקטרונים כדי להשיג יציבות
 שיתוף פעולה בין אטומים
שיתוף פעולה בין אטומים
אנלוגיה - שותפים לדירה
דמיינו שני שותפים לדירה שלכל אחד חסר חצי דירה. במקום שכל אחד ישכור דירה שלמה לבד, הם משתפים דירה אחת - ושניהם מרוויחים.
בדיוק כך עובד הקשר השיתופי: שני אטומים שכל אחד חסר להם אלקטרונים משתפים את האלקטרונים ביניהם, וכך שניהם מגיעים לקליפה מלאה.
 איך נוצר קשר שיתופי?
איך נוצר קשר שיתופי?
קשר שיתופי נוצר כאשר שני אטומים של אל-מתכות משתפים ביניהם אלקטרונים מהקליפה החיצונית.
כשני אטומים מתקרבים, האלקטרונים של אטום אחד נמשכים לגרעין של האטום השני, ולהפך.
נוצר מצב שבו זוג אלקטרונים משותף לשני האטומים - כל אלקטרון נמשך לשני הגרעינים.
תהליך זה מביא את שני האטומים למצב יציב יותר, כי כעת לכל אחד מהם קליפה חיצונית מלאה (או קרובה לכך).
הקשר נוצר בין אל-מתכות בלבד - כי לאל-מתכות יש נטייה לקבל אלקטרונים, לא לתת. כששניהם רוצים לקבל, הפתרון הוא לשתף.
הקשר השיתופי הוא שיתוף זוגות אלקטרונים בין אטומים של אל-מתכות, כך ששניהם משיגים קליפה חיצונית מלאה.
 סוגי קשרים שיתופיים
סוגי קשרים שיתופיים
לא כל הקשרים השיתופיים זהים. מספר זוגות האלקטרונים המשותפים קובע את סוג הקשר ואת חוזקו:
קשר יחיד
שיתוף זוג אלקטרונים אחד
זוג אלקטרונים אחד משותף.
סימון: קו אחד (-)
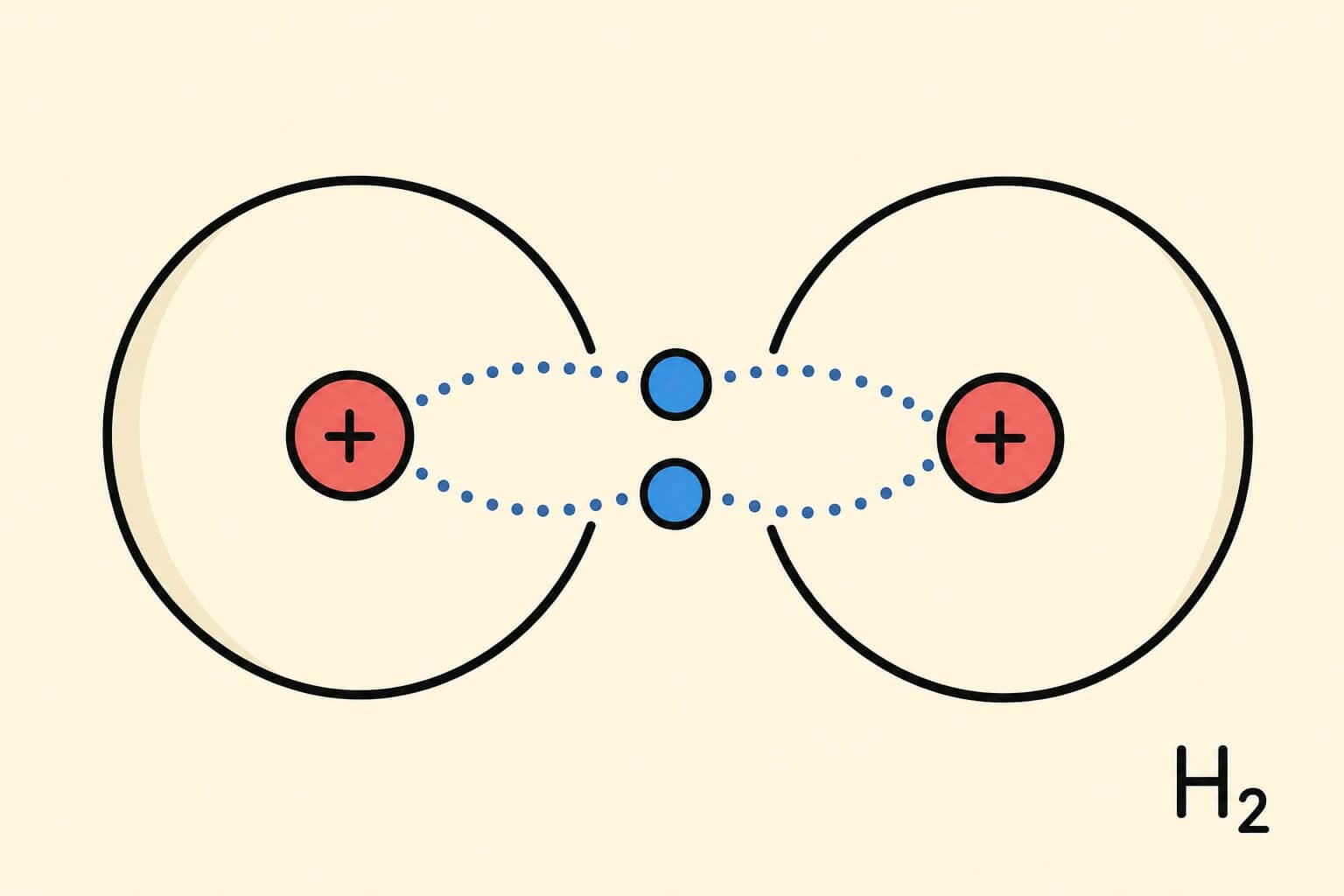
דוגמה: H-H (מולקולת מימן)
הקשר החלש ביותר מבין השלושה.
קשר כפול
שיתוף שני זוגות אלקטרונים
שני זוגות אלקטרונים משותפים.
סימון: שני קווים (=)
דוגמה: O=O (מולקולת חמצן)
חזק יותר מקשר יחיד.
קשר משולש
שיתוף שלושה זוגות אלקטרונים
שלושה זוגות אלקטרונים משותפים.
סימון: שלושה קווים
דוגמה: מולקולת חנקן (N)
החזק ביותר - קשה מאוד לנתק.
השוואת חוזק קשרים שיתופיים
| סוג קשר | זוגות אלקטרונים | חוזק יחסי | דוגמה | אנרגיה (קילוג'ול/מול) |
|---|---|---|---|---|
| יחיד (-) | 1 | חלש | H-H (מימן) | ~436 |
| כפול (=) | 2 | בינוני-חזק | O=O (חמצן) | ~498 |
| משולש | 3 | חזק מאוד | N≡N (חנקן) | ~945 |
* ככל שמספר זוגות האלקטרונים המשותפים גדול יותר, הקשר חזק יותר וקצר יותר
 דוגמאות למולקולות שיתופיות
דוגמאות למולקולות שיתופיות
 מולקולות שיתופיות נפוצות
מולקולות שיתופיות נפוצות
מולקולת מימן (H2)
כל אטום מימן צריך אלקטרון אחד נוסף (להשלמה ל-2).
שני אטומי מימן משתפים זוג אלקטרונים אחד.
נוצר קשר יחיד: H-H
מולקולת חמצן (O2)
כל אטום חמצן צריך 2 אלקטרונים נוספים (להשלמה ל-8).
שני אטומי חמצן משתפים שני זוגות אלקטרונים.
נוצר קשר כפול: O=O
מולקולת מים (H2O)
חמצן צריך 2 אלקטרונים, כל מימן צריך 1 אלקטרון.
לכן חמצן יוצר שני קשרים - אחד עם כל מימן.
H-O-H
מולקולת פחמן דו-חמצני (CO2)
פחמן צריך 4 אלקטרונים, כל חמצן צריך 2.
פחמן יוצר קשר כפול עם כל חמצן.
O=C=O
 קשרים שיתופיים בעולם האמיתי
קשרים שיתופיים בעולם האמיתי
 היכן פוגשים קשרים שיתופיים?
היכן פוגשים קשרים שיתופיים?
רוב החומרים שאנחנו מכירים מחיי היום-יום בנויים מקשרים שיתופיים:
- מים (H2O) - הנוזל הכי חשוב בטבע, בנוי מקשרים שיתופיים בין חמצן למימן
- האוויר שאנחנו נושמים - מולקולות חמצן (O2) וחנקן (N2) עם קשרים שיתופיים
- סוכר (C12H22O11) - כל הקשרים בו שיתופיים בין פחמן, מימן וחמצן
- DNA - החומר הגנטי שלנו בנוי ממולקולות עם אלפי קשרים שיתופיים
- פלסטיק, בגדים, תרופות - כולם מבוססי קשרים שיתופיים
 טעות נפוצה - לא לבלבל!
טעות נפוצה - לא לבלבל!
תלמידים רבים מבלבלים בין שיתוף למעבר אלקטרונים. הנה הדרך לזכור:
- קשר שיתופי = שיתוף (כמו לשתף סרט עם חבר - שניכם רואים)
- קשר יוני = מעבר (כמו לתת מתנה - רק אחד מקבל)
- אל-מתכת + אל-מתכת = שיתוף (שניהם רוצים לקבל, אז משתפים)
- מתכת + אל-מתכת = מעבר (המתכת מוותרת, האל-מתכת מקבלת)
שימו לב: הקשר השיתופי נוצר בין אל-מתכות בלבד. כשמתכת ואל-מתכת נפגשות, נוצר סוג אחר של קשר - הקשר היוני, אותו נלמד בשיעור הבא.
 סימולציה - יצירת קשר שיתופי
סימולציה - יצירת קשר שיתופי
בסימולציה הבאה תוכלו לראות כיצד אטומים של אל-מתכות משתפים אלקטרונים ביניהם כדי ליצור קשרים שיתופיים. נסו ליצור מולקולות שונות וצפו בשיתוף האלקטרונים.
 שאלה לחשיבה
שאלה לחשיבה
למה שני אטומי חנקן (N) יוצרים קשר משולש ביניהם ולא קשר יחיד?
לאטום חנקן יש 5 אלקטרוני ערכיות, ולכן הוא צריך 3 אלקטרונים נוספים כדי להשלים ל-8. כדי שכל אחד מהאטומים ישיג את 3 האלקטרונים החסרים, הם חייבים לשתף 3 זוגות אלקטרונים - ולכן נוצר קשר משולש, שהוא קשר חזק מאוד.
 שאלה לחשיבה
שאלה לחשיבה
מולקולת מתאן (CH4) מכילה 4 קשרים בין פחמן למימן. מדוע כל הקשרים הם יחידים ולא כפולים?
לפחמן יש 4 אלקטרוני ערכיות ויכולת קישור 4. כל אטום מימן צריך רק אלקטרון אחד (להשלמה ל-2). לכן כל קשר בין פחמן למימן דורש שיתוף של זוג אלקרטונים אחד בלבד - קשר יחיד. ארבעת הקשרים היחידים ממלאים בדיוק את יכולת הקישור של הפחמן.
 שאלה לחשיבה
שאלה לחשיבה
האוויר מכיל בעיקר חנקן (N2) וחמצן (O2). מדוע שני הגזים האלה לא מגיבים זה עם זה בתנאים רגילים, למרות שהם נמצאים יחד?
הקשר המשולש במולקולת חנקן הוא חזק מאוד (945 קילוג'ול/מול) וקשה לנתק אותו. גם הקשר הכפול בחמצן חזק (498 קילוג'ול/מול). בתנאים רגילים אין מספיק אנרגיה כדי לשבור את הקשרים הללו ולהתחיל תגובה. רק בטמפרטורות גבוהות מאוד (כמו בברק או במנוע רכב) יש מספיק אנרגיה לנתק את הקשרים ולגרום לתגובה.
ככל שמספר זוגות האלקטרונים המשותפים גדול יותר, הקשר חזק יותר וקשה יותר לנתק אותו:
- קשר יחיד - הכי חלש (~350 קילוג'ול/מול בממוצע)
- קשר כפול - חזק יותר (~600 קילוג'ול/מול בממוצע)
- קשר משולש - הכי חזק (~900 קילוג'ול/מול בממוצע)
לכן מולקולת חנקן (N2) עם הקשר המשולש שלה היא מולקולה יציבה מאוד, ולשבירת הקשר שלה נדרשת אנרגיה רבה. זו הסיבה שחנקן הוא גז אינרטי יחסית באוויר (78% מהאוויר!).
עובדה מפתיעה: היהלום, החומר הקשה ביותר בטבע, בנוי מאטומי פחמן בלבד - כל פחמן מחובר ל-4 פחמנים שכנים בקשרים שיתופיים יחידים. המבנה הזה, שנקרא 'סריג יהלום', יוצר חומר קשיח להפליא.
כמעט כל המולקולות החשובות לחיים בנויות מקשרים שיתופיים:
- DNA - שרשרת ארוכה של אטומי פחמן, חמצן, חנקן ומימן מחוברים בקשרים שיתופיים. כל תא בגופנו מכיל כ-2 מטר של DNA!
- חלבונים - שרשראות של חומצות אמינו, מחוברות בקשר שיתופי שנקרא 'קשר פפטידי'
- גלוקוז (C6H12O6) - מולקולת הסוכר שמספקת אנרגיה לכל תא, בנויה כולה מקשרים שיתופיים
אפשר לומר שהקשר השיתופי הוא 'הדבק' שמחזיק את החיים יחד!
 מה הלאה?
מה הלאה?
בשיעור הבא נלמד על הסוג השני של קשר כימי - הקשר היוני. נראה מה קורה כשמתכת פוגשת אל-מתכת - במקום שיתוף, מתרחש מעבר אלקטרונים. מוכנים?