יכולת קישור
כמה קשרים כל אטום יכול ליצור?
 הכלל הפשוט
הכלל הפשוט
אנלוגיה - כמה ידיים חופשיות?
דמיינו שכל אטום הוא אדם עם ידיים. יכולת הקישור אומרת כמה ידיים חופשיות יש לו כדי ללחוץ ידיים עם אטומים אחרים.
לפחמן יש 4 ידיים חופשיות - הוא יכול ללחוץ ידיים עם 4 אטומים!
לחמצן יש 2 ידיים חופשיות - הוא יכול ללחוץ ידיים עם 2 אטומים.
למימן יש יד אחת חופשית - הוא יכול ללחוץ ידיים עם אטום אחד בלבד.
לגזים אצילים אין ידיים חופשיות - הם מסתדרים לבד!
 מדריך חישוב יכולת קישור - צעד אחר צעד
מדריך חישוב יכולת קישור - צעד אחר צעד
 3 השלבים לחישוב יכולת קישור
3 השלבים לחישוב יכולת קישור
עקבו אחרי השלבים הבאים לחישוב יכולת קישור של כל יסוד:
- מצאו באיזה טור נמצא היסוד בטבלה המחזורית - מספר הטור = מספר אלקטרוני הערכיות
- חשבו: 8 - מספר אלקטרוני ערכיות = יכולת קישור
- בדקו חריגים: מימן - יכולת קישור 1 (השלמה ל-2, לא ל-8), גזים אצילים - יכולת קישור 0 (קליפה מלאה)
יכולת קישור של יסודות נפוצים
| יסוד | סימן | טור | אלקטרוני ערכיות | חישוב | יכולת קישור |
|---|---|---|---|---|---|
| מימן | H | 1 | 1 | 2 - 1 | 1 |
| פחמן | C | 4 | 4 | 8 - 4 | 4 |
| חנקן | N | 5 | 5 | 8 - 5 | 3 |
| חמצן | O | 6 | 6 | 8 - 6 | 2 |
| פלואור | F | 7 | 7 | 8 - 7 | 1 |
| כלור | Cl | 7 | 7 | 8 - 7 | 1 |
| גופרית | S | 6 | 6 | 8 - 6 | 2 |
| נאון | Ne | 8 (18) | 8 | 8 - 8 | 0 (יציב) |
* מימן חריג - יכולת הקישור שלו היא 1, כי הקליפה הראשונה מכילה רק 2 אלקטרונים
 כלל חשוב
כלל חשוב
יסודות באותו טור בטבלה המחזורית מכילים אותו מספר אלקטרוני ערכיות, ולכן יש להם אותה יכולת קישור.
לדוגמה: כלור (Cl) ופלואור (F) שניהם בטור 7 - ולשניהם יכולת קישור 1.
 טיפ לחישוב מהיר
טיפ לחישוב מהיר
אם אתם יודעים באיזה טור נמצא היסוד, תוכלו לחשב את יכולת הקישור מיד:
- טורים 1-4: יכולת קישור = מספר הטור (1, 2, 3, 4)
- טורים 5-7: יכולת קישור = 8 - מספר הטור (3, 2, 1)
- טור 8 (18): יכולת קישור = 0 (גזים אצילים)
- שימו לב: טור 4 = יכולת קישור 4 (המקסימום!)
 טעויות נפוצות - הימנעו!
טעויות נפוצות - הימנעו!
תלמידים רבים טועים בנקודות הבאות:
- מימן הוא חריג - ההשלמה היא ל-2, לא ל-8. יכולת קישור 1
- גזים אצילים (He, Ne, Ar) - הקליפה שלהם כבר מלאה, יכולת קישור 0
- אל תחשבו את כל האלקטרונים - רק את אלקטרוני הערכיות (קליפה חיצונית)
- יכולת קישור מקסימלית היא 4 (פחמן) - אין יכולת קישור 5, 6 או 7
 איך מציירים מבנה לואיס?
איך מציירים מבנה לואיס?
מבנה לואיס הוא שיטה לציור מולקולות שמראה את אלקטרוני הערכיות. כל קו מייצג זוג אלקטרונים משותפים (קשר), וכל זוג נקודות מייצג זוג אלקטרונים בלתי קושרים.
 שלבים לציור מבנה לואיס
שלבים לציור מבנה לואיס
עקבו אחרי השלבים הבאים לציור מבנה לואיס של כל מולקולה:
- חשבו את יכולת הקישור של כל אטום במולקולה
- הניחו את האטום המרכזי באמצע (האטום עם יכולת הקישור הגבוהה ביותר)
- חברו את האטומים החיצוניים אליו בקווים (כל קו = זוג אלקטרונים משותפים)
- ודאו שכל אטום מגיע ל-8 אלקטרונים (או 2 למימן)
- סמנו זוגות אלקטרונים בלתי קושרים כנקודות
 תרגול מבנה לואיס
תרגול מבנה לואיס
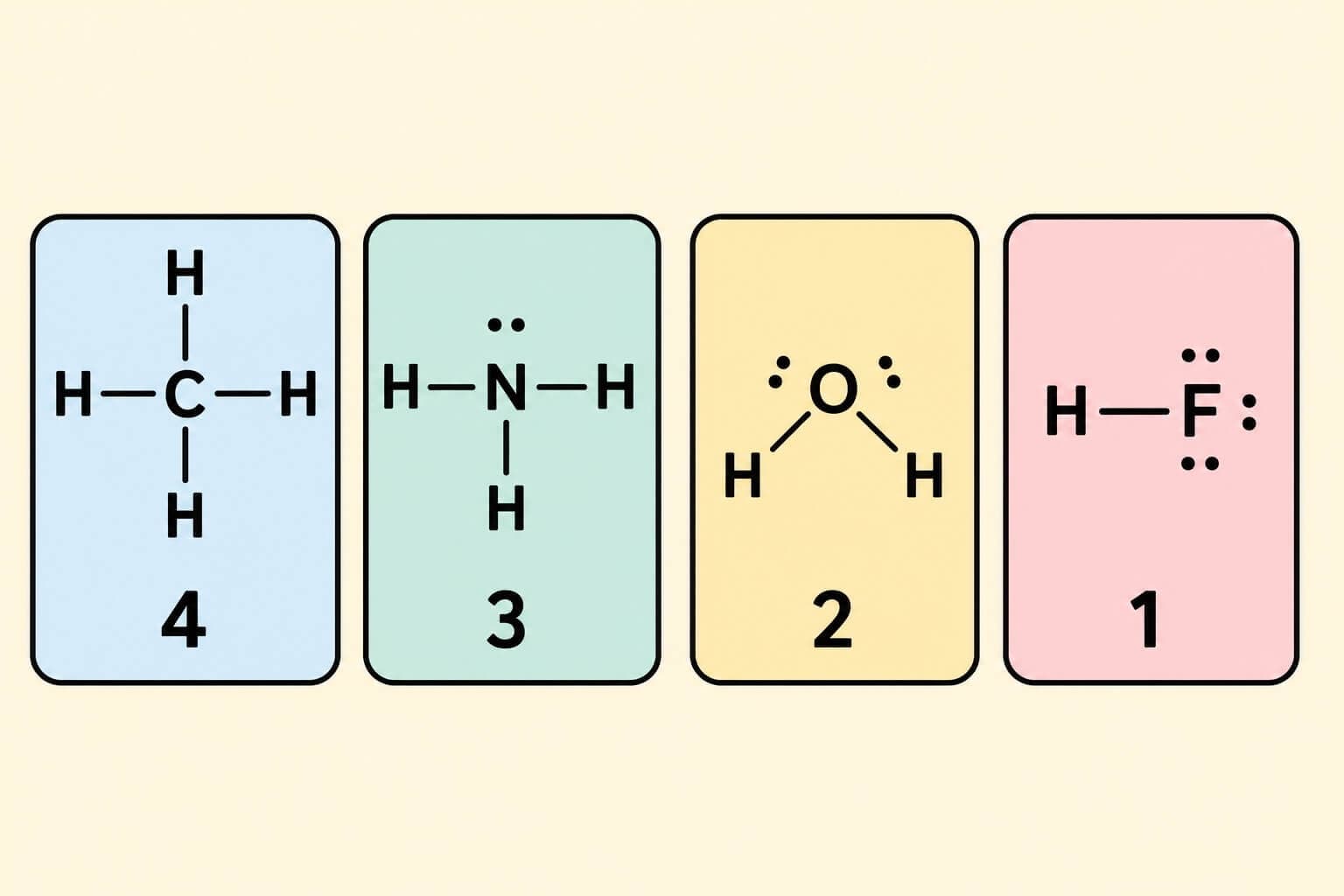
מים (H2O)
חמצן: יכולת קישור 2
מימן: יכולת קישור 1
לכן חמצן יוצר 2 קשרים, אחד עם כל מימן.
H - O - H
לחמצן נשארים עוד 2 זוגות אלקטרונים בלתי קושרים.
אמוניה (NH3)
חנקן: יכולת קישור 3
מימן: יכולת קישור 1
לכן חנקן יוצר 3 קשרים, אחד עם כל מימן.
לחנקן נשאר זוג אלקטרונים בלתי קושר אחד.
מתאן (CH4)
פחמן: יכולת קישור 4
מימן: יכולת קישור 1
לכן פחמן יוצר 4 קשרים, אחד עם כל מימן.
לפחמן לא נשארים אלקטרונים בלתי קושרים.
פחמן דו-חמצני (CO2)
פחמן: יכולת קישור 4
חמצן: יכולת קישור 2
פחמן יוצר קשר כפול עם כל חמצן (2+2=4 קשרים).
O = C = O
 למה הפחמן כל כך מיוחד?
למה הפחמן כל כך מיוחד?
פחמן - האטום הרב-תכליתי
לפחמן יש יכולת קישור 4 - הגבוהה ביותר בין היסודות הנפוצים. מה הופך את זה למיוחד?
1. שרשראות: פחמן יכול להתחבר לאטומי פחמן אחרים בשרשראות ארוכות: C-C-C-C-C...
2. ענפים: כל פחמן בשרשרת יכול ליצור ענפים לצדדים.
3. טבעות: שרשרת פחמן יכולה להתעקל ולסגור טבעת (כמו בנזן).
4. קשרים כפולים ומשולשים: פחמן יכול ליצור קשרים כפולים (C=C) ומשולשים.
בזכות כל האפשרויות האלה, קיימים מיליוני תרכובות פחמן שונות! כל הכימיה האורגנית - תרופות, פלסטיק, דלקים, מזון - מבוססת על פחמן.
 סימולציה - כלל האוקטט
סימולציה - כלל האוקטט
בסימולציה הבאה תוכלו לחקור את כלל האוקטט - לראות כיצד אטומים שונים שואפים להשלים 8 אלקטרונים בקליפה החיצונית, וכיצד הם עושים זאת על ידי יצירת קשרים.
 סימולציה - יציבות הגזים האצילים
סימולציה - יציבות הגזים האצילים
מדוע הגזים האצילים לא יוצרים קשרים? בסימולציה הבאה תוכלו לראות את הסיבה - הקליפה החיצונית שלהם כבר מלאה.
 שאלה לחשיבה
שאלה לחשיבה
לפחמן יש יכולת קישור 4 ולמימן יכולת קישור 1. איזו נוסחה מולקולרית מתקבלת כשפחמן קושר רק אטומי מימן?
CH4 - מתאן. פחמן צריך 4 קשרים, וכל מימן יכול ליצור קשר אחד. לכן צריך 4 אטומי מימן כדי להשלים את 4 הקשרים של הפחמן.
שימו לב: יכולת הקישור של פחמן (4) תהיה חשובה מאוד כשנלמד על כימיה אורגנית בפרק 3.
 שאלה לחשיבה
שאלה לחשיבה
גופרית (S) נמצאת בטור 6, כמו חמצן. האם המולקולה H2S (מימן גופרי) דומה במבנה למולקולת H2O? הסבירו.
כן! גופרית, כמו חמצן, נמצאת בטור 6 ולכן יכולת הקישור שלה היא 2 (8-6=2). בדיוק כמו שחמצן יוצר 2 קשרים עם מימן במים (H-O-H), גופרית יוצרת 2 קשרים עם מימן ב-H2S (H-S-H). המבנה דומה מאוד! זו דוגמה לכך שיסודות באותו טור מתנהגים באופן דומה.
 שאלה לחשיבה
שאלה לחשיבה
יסוד X נמצא בטור 3 ויסוד Y נמצא בטור 7. מהי הנוסחה של המולקולה שתיווצר ביניהם (בקשר שיתופי)?
ליסוד X יכולת קישור 3 (8-3=5... לא! טור 3 = 3 אלקטרוני ערכיות, יכולת קישור = 8-3=5... רגע, בטורים 1-4 יכולת הקישור שווה למספר הטור, כלומר 3). ליסוד Y יכולת קישור 1 (8-7=1). לכן X צריך 3 קשרים ו-Y יכול ליצור קשר 1, ולכן הנוסחה היא XY3.
גילברט ניוטון לואיס (1875-1946) היה כימאי אמריקאי שפיתח את שיטת הציור שנקראת על שמו. בשנת 1916 הוא הציע שקשר כימי נוצר כאשר אטומים משתפים זוגות אלקטרונים.
הרעיון שלו היה מהפכני - לפניו, אף אחד לא הבין למה אטומים מתחברים זה לזה. לואיס הראה שהתשובה קשורה לאלקטרונים בקליפה החיצונית ולשאיפה להשלים אותה ל-8.
למרות שלואיס מעולם לא זכה בפרס נובל, הרעיונות שלו משמשים כל תלמיד כימיה בעולם עד היום!
 מה הלאה?
מה הלאה?
עכשיו שאנחנו יודעים כמה קשרים כל אטום יכול ליצור, נוכל ללמוד את שפת הכימיה - כיצד כותבים נוסחאות כימיות ומייצגים תהליכים כימיים. בשיעור הבא נלמד לקרוא ולכתוב בשפה הבינלאומית של הכימאים!