הקשר היוני
כאשר אטומים מעבירים אלקטרונים ונוצרים יונים
 מתכת פוגשת אל-מתכת
מתכת פוגשת אל-מתכת
אנלוגיה - אימוץ אלקטרון
דמיינו שלמשפחה אחת (מתכת) יש ילד אחד עודף שהם לא מצליחים לטפל בו, ולמשפחה שנייה (אל-מתכת) חסר ילד כדי להשלים את המשפחה.
הפתרון? אימוץ - הילד עובר ממשפחה אחת לשנייה, ושתי המשפחות מרוצות.
בקשר יוני קורה בדיוק אותו דבר: המתכת 'מאמצת' את האלקטרון שלה לאל-מתכת. שניהם מגיעים לקליפה מלאה ומרוצים!
 איך נוצר קשר יוני?
איך נוצר קשר יוני?
קשר יוני נוצר כאשר מתכת מעבירה אלקטרונים לאל-מתכת, ונוצרים יונים בעלי מטען הפוך שנמשכים זה לזה.
שלב 1: אטום המתכת (למשל, נתרן) מאבד אלקטרון מהקליפה החיצונית ← הופך לקטיון (יון חיובי, Na+).
שלב 2: אטום האל-מתכת (למשל, כלור) קולט את האלקטרון ← הופך לאניון (יון שלילי, Cl-).
שלב 3: כוח המשיכה החשמלי בין Na+ ל-Cl- יוצר את הקשר היוני.
למה המתכת מוותרת?
לנתרן יש רק אלקטרון אחד בקליפה החיצונית. קל יותר לו להיפטר ממנו (ולחשוף קליפה מלאה) מאשר להשיג עוד 7.
קשר יוני = מעבר אלקטרונים ← יצירת יונים ← משיכה חשמלית בין יונים הפוכים.
 קטיון מול אניון
קטיון מול אניון
 קטיון (יון חיובי)
קטיון (יון חיובי)
נוצר כשאטום מאבד אלקטרונים.
יש לו יותר פרוטונים מאלקטרונים.
נוצר בדרך כלל ממתכות.
דוגמה: Na ← Na+ (נתרן איבד אלקטרון אחד)
 אניון (יון שלילי)
אניון (יון שלילי)
נוצר כשאטום קולט אלקטרונים.
יש לו יותר אלקטרונים מפרוטונים.
נוצר בדרך כלל מאל-מתכות.
דוגמה: Cl ← Cl- (כלור קלט אלקטרון אחד)
 איך לזכור? קטיון = חתול!
איך לזכור? קטיון = חתול!
טריק לזכירה: קטיון נשמע כמו 'cat' (חתול באנגלית). חתול הוא חיובי ומחבק - יון חיובי!
- קטיון = cat = חיובי (+)
- אניון = a-negative = שלילי (-)
- מתכת מאבדת ← נהפכת לקטיון (+)
- אל-מתכת קולטת ← נהפכת לאניון (-)
 סימולציה - יצירת יונים
סימולציה - יצירת יונים
בסימולציה הבאה תוכלו לראות כיצד אטומים מאבדים או קולטים אלקטרונים כדי להפוך ליונים. צפו בתהליך המעבר של אלקטרונים ממתכת לאל-מתכת.
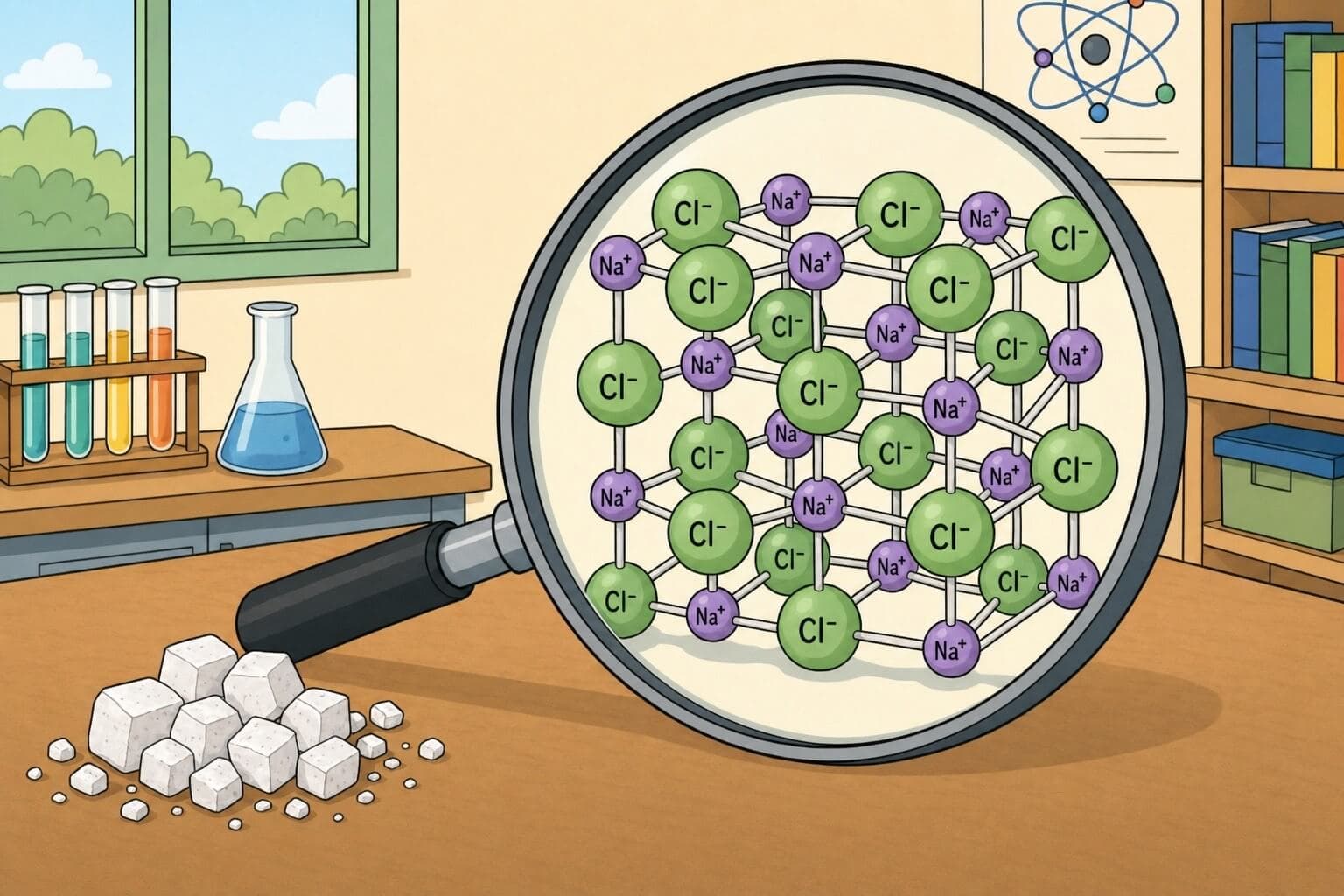
 הסריג היוני - מבנה תלת-ממדי
הסריג היוני - מבנה תלת-ממדי
בתרכובת יונית, היונים לא קיימים בזוגות בודדים. הם מסודרים בסריג יוני - מבנה תלת-ממדי מסודר שבו כל יון מוקף ביונים בעלי מטען הפוך.
אנלוגיה - סריג יוני כמו ריצוף שחמט
דמיינו לוח שחמט תלת-ממדי ענק. המשבצות השחורות מייצגות יונים חיוביים (+) והלבנות יונים שליליים (-).
כל משבצת שחורה מוקפת במשבצות לבנות, וכל לבנה מוקפת בשחורות. בדיוק כך בסריג יוני: כל יון חיובי מוקף ביונים שליליים, וכל שלילי מוקף בחיוביים.
הסידור המסודר הזה מחזיק את המבנה ביחד בזכות כוחות המשיכה החשמליים.
דוגמה: מלח שולחן (NaCl)
מלח שולחן (נתרן כלורי) הוא דוגמה קלאסית לתרכובת יונית.
בסריג של NaCl, כל יון Na+ מוקף ב-6 יוני Cl- וכל יון Cl- מוקף ב-6 יוני Na+.
המבנה המסודר הזה הוא שנותן לגבישים של מלח את צורתם המעוקבת האופיינית.
למעשה, כשאתם שופכים מלח על הבשר, אתם רואים מיליארדי יונים מסודרים בסריג מושלם!
 תכונות תרכובות יוניות
תכונות תרכובות יוניות
תכונות אופייניות
טמפרטורות התכה גבוהות
המשיכה בין היונים חזקה מאוד, ולכן נדרש חימום רב כדי לשבור את המבנה. למשל, NaCl נמס ב-801 מעלות!
מוליכות חשמל בתמיסה
בתמיסה או בהיתוך, היונים חופשיים לנוע ומוליכים חשמל. במצב מוצק - לא, כי היונים נעולים בסריג.
מסיסות במים
רוב התרכובות היוניות מסיסות במים, כי מולקולות המים מפרידות בין היונים ו'עוטפות' כל יון.
שבירות
הסריג היוני שביר - מכה חזקה מסיטה שכבה שלמה. יונים בעלי אותו מטען נפגשים, דוחים, והגביש נשבר.
 מלח בחיי היום-יום
מלח בחיי היום-יום
מלח שולחן (NaCl)
לא רק תיבול! מלח חיוני לגוף האדם:
- העברת אותות עצביים
- שמירה על לחץ דם תקין
- ויסות נוזלים בגוף
סידן כלורי (CaCl2)
משמש להתכת קרח על כבישים בחורף.
מוריד את טמפרטורת ההקפאה של מים.
גם בתהליך הכנת גבינה!
סידן פחמתי (CaCO3)
מרכיב עיקרי של:
- גיר (על הלוח)
- שיש (מדרגות, פסלים)
- צדפות ושלדי אלמוגים
נתרן פחמתי (NaHCO3)
סודה לשתייה:
- אבקת אפייה בעוגות
- סותר חומציות בבטן
- ניקוי משטחים
 מתי נוצר קשר יוני ומתי שיתופי?
מתי נוצר קשר יוני ומתי שיתופי?
 קשר יוני מול קשר שיתופי
קשר יוני מול קשר שיתופי
 קשר יוני
קשר יוני
בין מתכת לאל-מתכת.
מעבר אלקטרונים.
נוצרים יונים וסריג.
טמפרטורת התכה גבוהה.
מוליך בתמיסה.
דוגמה: מתכת + אל-מתכת ← קשר יוני
 קשר שיתופי
קשר שיתופי
בין אל-מתכת לאל-מתכת.
שיתוף אלקטרונים.
נוצרות מולקולות.
טמפרטורת התכה נמוכה.
לא מוליך חשמל.
דוגמה: אל-מתכת + אל-מתכת ← קשר שיתופי
הכלל הפשוט: מתכת + אל-מתכת = יוני, אל-מתכת + אל-מתכת = שיתופי
 סימולציה - הקשר היוני
סימולציה - הקשר היוני
בסימולציה הבאה תוכלו לחקור את הקשר היוני - לראות כיצד מתכת ואל-מתכת יוצרות קשר על ידי מעבר אלקטרונים, ומה קורה כשהיונים מתקרבים זה לזה.
 שאלה לחשיבה
שאלה לחשיבה
מדוע תרכובות יוניות מוליכות חשמל בתמיסה אבל לא במצב מוצק?
במצב מוצק, היונים נעולים במקומם בסריג היוני ולא יכולים לנוע. חשמל הוא תנועה של מטענים, ואם המטענים לא זזים - אין הולכה. בתמיסה, המים מפרקים את הסריג והיונים חופשיים לנוע - ולכן הם מוליכים חשמל.
 שאלה לחשיבה
שאלה לחשיבה
מגנזיום (Mg) נמצא בטור 2. כמה אלקטרונים הוא יאבד ביצירת קשר יוני, ומהו היון שייווצר?
מגנזיום בטור 2, כלומר יש לו 2 אלקטרוני ערכיות. הוא יאבד את שניהם כדי לחשוף קליפה פנימית מלאה. היון שייווצר: Mg2+ (קטיון עם מטען +2). לדוגמה, בתרכובת MgO: מגנזיום מאבד 2 אלקטרונים (Mg2+) וחמצן קולט 2 (O2-), ולכן היחס הוא 1:1.
 שאלה לחשיבה
שאלה לחשיבה
מדוע גביש מלח שביר, אבל חוט נחושת (מתכת) ניתן לכפוף?
בגביש יוני, מכה מסיטה שכבה שלמה של יונים. כשהשכבה זזה, פתאום יונים חיוביים ניצבים מול חיוביים - הדחייה גורמת לשבירה. בנחושת, האלקטרונים משוטטים חופשי ויכולים 'להתאים' לכל סידור חדש. לכן מתכות גמישות ותרכובות יוניות שבירות.
תרכובות יוניות נמצאות בכל מקום:
- מלח שולחן (NaCl) - תיבול מזון ושימור
- סידן כלורי (CaCl2) - התכת קרח על כבישים
- סידן פחמתי (CaCO3) - גיר, שיש, צדפות
- נתרן פחמתי (NaHCO3) - סודה לשתייה
- פלואוריד נתרן (NaF) - במשחת שיניים - מחזק אמייל
- אשלגן יודיד (KI) - מוסף למלח למניעת מחלות בלוטת התריס
למעשה, גם הגוף שלנו תלוי ביונים: יוני נתרן (Na+) ואשלגן (K+) אחראים על העברת אותות עצביים, ויוני סידן (Ca2+) חיוניים לבניית עצמות.
ים המלח הוא המקום הנמוך ביותר בעולם (כ-430 מטר מתחת לפני הים) ומכיל ריכוז מלח של כ-34% - פי 10 ממי ים רגילים!
המלחים ב'ים המלח' הם בעיקר תרכובות יוניות: NaCl (מלח רגיל), MgCl2 (מגנזיום כלורי), ו-KCl (אשלגן כלורי). הריכוז הגבוה של היונים במים הוא שמאפשר ציפה קלה - המים הצפופים 'דוחפים' אתכם למעלה!
 מה הלאה?
מה הלאה?
עכשיו שאנחנו מכירים את שני סוגי הקשרים (שיתופי ויוני), בשיעור הבא נלמד על יכולת קישור - כמה קשרים כל אטום יכול ליצור, ואיך מחשבים את זה.