סיכום - הקשר הכימי
חזרה על כל מה שלמדנו על כוחות בין אטומים
 מושגי מפתח
מושגי מפתח
כוחות חשמליים
כוח משיכה: בין מטענים הפוכים (+ ו-)
כוח דחייה: בין מטענים זהים
הכוחות שמחזיקים את מבנה האטום.
אלקטרוני ערכיות
אלקטרונים בקליפה החיצונית.
קובעים את ההתנהגות הכימית.
מספרם = מספר הטור בטבלה.
כלל האוקטט
אטומים שואפים ל8 אלקטרונים בקליפה החיצונית.
מימן: השלמה ל-2.
זו הסיבה ליצירת קשרים.
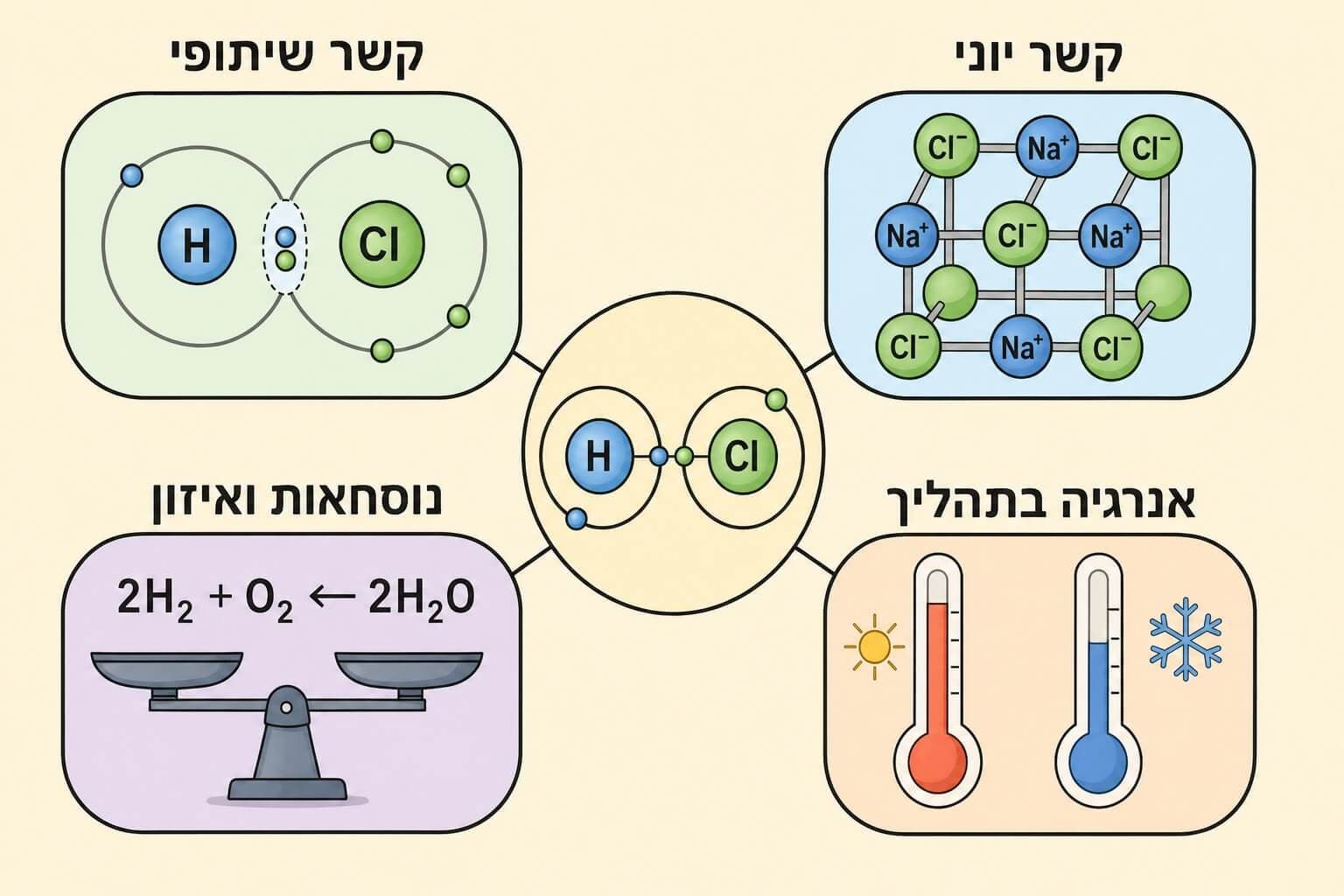
 קשר שיתופי מול קשר יוני
קשר שיתופי מול קשר יוני
 קשר שיתופי (קוולנטי)
קשר שיתופי (קוולנטי)
בין אל-מתכת לאל-מתכת
שיתוף אלקטרונים
נוצרות מולקולות
סוגים: יחיד, כפול, משולש
דוגמה: H2O, CO2, O2, NH3
 קשר יוני
קשר יוני
בין מתכת לאל-מתכת
מעבר אלקטרונים
נוצרים יונים וסריג יוני
תכונות: טמפרטורת התכה גבוהה, שבירות
דוגמה: NaCl, MgO, CaCl2
יכולת קישור - סיכום
| יסוד | אלקטרוני ערכיות | יכולת קישור |
|---|---|---|
| H (מימן) | 1 | 1 |
| C (פחמן) | 4 | 4 |
| N (חנקן) | 5 | 3 |
| O (חמצן) | 6 | 2 |
| F, Cl (הלוגנים) | 7 | 1 |
| He, Ne (גזים אצילים) | 2 או 8 | 0 |
* נוסחה: יכולת קישור = 8 - מספר אלקטרוני ערכיות (למימן: 2 - 1 = 1)
 נוסחאות ותהליכים כימיים
נוסחאות ותהליכים כימיים
מושגים בשפת הכימיה
נוסחה מולקולרית
מציגה אילו אטומים וכמה מכל סוג. דוגמה: H2O = 2 מימן + 1 חמצן.
משוואה כימית
מגיבים ← תוצרים. חייבת להיות מאוזנת (חוק שימור המסה).
מקדם
מספר גדול לפני הנוסחה. מציין כמה מולקולות. דוגמה: 2H2O = 2 מולקולות מים.
אינדקס
מספר קטן למטה מימין. מציין כמה אטומים ביסוד. דוגמה: H2 = 2 אטומי מימן.
 אנרגיה בתהליכים כימיים
אנרגיה בתהליכים כימיים
 תהליך פולט מול קולט אנרגיה
תהליך פולט מול קולט אנרגיה
 פולט אנרגיה (אקסותרמי)
פולט אנרגיה (אקסותרמי)
אנרגיית יצירה > אנרגיית ניתוק
הסביבה מתחממת
דוגמה: בעירה, נשימה תאית, חלודה
 קולט אנרגיה (אנדותרמי)
קולט אנרגיה (אנדותרמי)
אנרגיית ניתוק > אנרגיית יצירה
הסביבה מתקררת
דוגמה: פוטוסינתזה, פירוק מים, בישול ביצה
זכרו: ניתוק קשר = השקעת אנרגיה, יצירת קשר = שחרור אנרגיה.
 בעירה - שלושת התנאים
בעירה - שלושת התנאים
חומר דליק
חומר שיכול לבעור: עץ, נייר, גז, בנזין.
חמצן
בדרך כלל מגיע מהאוויר (21% חמצן).
טמפרטורת הצתה
הטמפרטורה המינימלית לתחילת בעירה.
 טיפים למבחן
טיפים למבחן
 איך לזהות סוג קשר?
איך לזהות סוג קשר?
שאלו את עצמכם: מי היסודות שמשתתפים בקשר?
- מתכת + אל-מתכת = קשר יוני (מעבר אלקטרונים)
- אל-מתכת + אל-מתכת = קשר שיתופי (שיתוף אלקטרונים)
- מתכות נמצאות בצד שמאל של הטבלה, אל-מתכות בצד ימין
 איך לחשב יכולת קישור?
איך לחשב יכולת קישור?
הנוסחה הפשוטה: יכולת קישור = 8 - מספר אלקטרוני ערכיות
- מצאו את הטור בטבלה המחזורית = מספר אלקטרוני ערכיות
- חשבו: 8 - מספר אלקטרוני ערכיות = יכולת קישור
- חריג: מימן - יכולת קישור 1 (השלמה ל-2, לא ל-8)
- גזים אצילים: יכולת קישור 0 (קליפה מלאה)
 תחנת חזרה מהירה
תחנת חזרה מהירה
לפני המבחן המסכם עברו תחנת חזרה קצרה עם 6 משימות בלבד. בכל פעם תופיע משימה אחת, תקבלו פידבק מיידי, ותמשיכו בלי לגלול בתוך לוחות עמוסים.
 חידון בדיקה מהיר
חידון בדיקה מהיר
החידון כאן הוא קצר וממוקד - 10 שאלות שמוודאות שאתם שולטים ברעיונות המרכזיים של הפרק. אם תרצו את כל מאגר השאלות המסכם, עברו אחר כך למבחן המסכם המלא.
סידן (Ca, טור 2) וכלור (Cl, טור 7) יוצרים תרכובת יונית. מהי הנוסחה?
תרגול מתקדם
מוכנים למבחן המסכם המלא?
עברו לחידון המורחב של הפרק לתרגול מקיף עם 104 שאלות מכל נושאי הלימוד.