מבוא לחומצות ובסיסים
שני סוגים של חומרים עם תכונות הפוכות - יסודות הכימיה של תמיסות
 הרחבה
הרחבה
פרק זה הוא תוכן הרחבה (רשות). הוא מרחיב ומעמיק את הידע שנלמד בכיתה ח' על חומצות, בסיסים ותמיסות.
 חומצות ובסיסים סביבנו
חומצות ובסיסים סביבנו
 מה הן חומצות ומה הם בסיסים?
מה הן חומצות ומה הם בסיסים?
נתחיל עם תרגיל מחשבה: דמיינו שאתם במטבח. על השולחן יש מיץ לימון, חומץ, סבון כלים, אקונומיקה, מים מהברז, ותרופה לצרבת. איך תחלקו אותם לקבוצות? אם אמרתם 'חמוץ מול חלקלק' או 'טבעי מול כימי', אתם על הדרך הנכונה. בכימיה, החלוקה המדויקת היא: חומצות מול בסיסים.
 חומצות מול בסיסים - תכונות מאפיינות
חומצות מול בסיסים - תכונות מאפיינות
 חומצות
חומצות
טעם חמוץ (אסור לטעום בניסוי!)
משחררות יוני הידרוניום (H3O+) במים
מגיבות עם מתכות ומשחררות גז מימן (בועות)
משנות צבע אינדיקטורים
מוליכות חשמל בתמיסה (אלקטרוליטים)
דוגמאות: חומץ, מיץ לימון, חומצת קיבה, ויטמין C
דוגמה: HCl ← H+ + Cl- (בתמיסה מימית)
 בסיסים
בסיסים
מרגישים חלקלקים למגע (אסור לגעת ללא ציוד!)
טעם מריר
משחררים יוני הידרוקסיל (OH-) במים
משנים צבע אינדיקטורים (כיוון הפוך מחומצות)
מוליכים חשמל בתמיסה
דוגמאות: סבון, אקונומיקה, סודה לשתייה, אמוניה
דוגמה: NaOH ← Na+ + OH- (בתמיסה מימית)
שני סוגי החומרים מוליכים חשמל בתמיסה כי הם יוצרים יונים חופשיים במים
 שאלה לחשיבה
שאלה לחשיבה
מדוע אסור לזהות חומצות ובסיסים על ידי טעימה במעבדה, למרות שחומצות טעמן חמוץ ובסיסים טעמם מריר?
חומצות ובסיסים חזקים (כמו HCl, H2SO4, NaOH) הם חומרים מסוכנים שגורמים לכוויות כימיות. טעימה עלולה לגרום לנזק חמור לפה, לוושט ולקיבה. במעבדה משתמשים באינדיקטורים, נייר pH או חיישנים דיגיטליים לזיהוי בטוח.
 יוני הידרוניום והידרוקסיל - המפתח להבנה
יוני הידרוניום והידרוקסיל - המפתח להבנה
 מה קובע אם תמיסה חומצית או בסיסית?
מה קובע אם תמיסה חומצית או בסיסית?
הסוד נמצא ביונים. ההבדל בין חומצה לבסיס נקבע על פי סוג היונים ששולטים בתמיסה.
כאשר חומצה מומסת במים, היא משחררת יוני מימן (H+). יון H+ בודד לא יכול להתקיים לבד במים - הוא מתחבר מיד למולקולת מים ויוצר יון הידרוניום (H3O+).
התהליך: HA + H2O ← H3O+ + A-
כאשר בסיס מומס במים, הוא משחרר יוני הידרוקסיל (OH-).
התהליך: BOH ← B+ + OH-
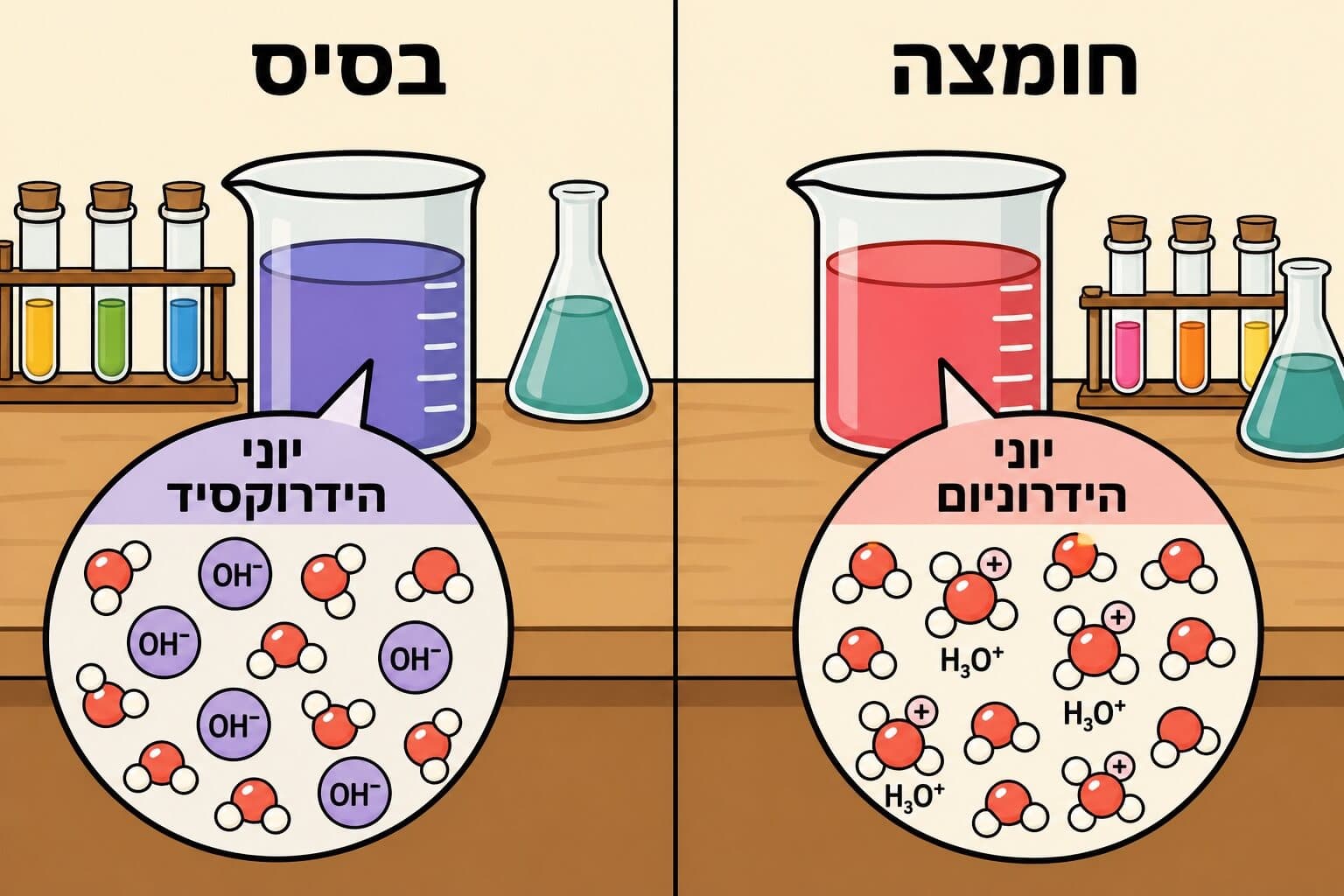
תמיסה חומצית: ריכוז H3O+ > ריכוז OH-
תמיסה בסיסית: ריכוז OH- > ריכוז H3O+
תמיסה ניטרלית: ריכוז H3O+ = ריכוז OH-
סוג היונים השולטים בתמיסה קובע אם היא חומצית, בסיסית או ניטרלית. יחס הריכוזים בין H3O+ ל-OH- הוא המפתח.
 עובדה מפתיעה
עובדה מפתיעה
גם במים טהורים לחלוטין קיימים יוני H3O+ ו-OH-! מולקולות מים מגיבות זו עם זו בתהליך שנקרא אוטופרוטוליזה: H2O + H2O ← H3O+ + OH-. אבל הריכוז זעיר - 10^-7 mol/L בלבד. לכן מים טהורים ניטרליים.
 דיסוציאציה - התפרקות ליונים במים
דיסוציאציה - התפרקות ליונים במים
דיסוציאציה היא תהליך שבו חומר מתפרק ליונים כשהוא מומס במים. כל חומצה וכל בסיס עוברים דיסוציאציה - אחרת לא היו משחררים יונים ולא היינו מרגישים את התכונות שלהם.
נקודה חשובה: לא כל חומצה מתפרקת באותה מידה. יש חומצות שכל המולקולות שלהן מתפרקות (דיסוציאציה מלאה), ויש כאלה שרק חלק קטן מתפרק (דיסוציאציה חלקית). נלמד על כך לעומק בשיעור הבא על דיסוציאציה.
 חומצות ובסיסים נפוצים
חומצות ובסיסים נפוצים
הנה סקירה של החומצות והבסיסים הנפוצים ביותר. שימו לב לנוסחה, למקור ולשימוש של כל אחד:
חומצות חזקות
חומצת מלח (HCl)
נמצאת בקיבה שלנו, בתעשייה
חומצה גופרתית (H2SO4)
מצברי מכוניות, דשנים
חומצה חנקתית (HNO3)
ייצור דשנים, חומרי נפץ
כולן עוברות דיסוציאציה מלאה
חומצות חלשות
חומצה ציטרית
בפירות הדר (לימון, תפוז)
חומצה אצטית (CH3COOH)
חומץ - חלקית בלבד
חומצה פחמתית (H2CO3)
משקאות מוגזים
חומצה אסקורבית
ויטמין C
עוברות דיסוציאציה חלקית
בסיסים נפוצים
נתרן הידרוקסיד (NaOH)
בסיס חזק, ייצור סבון
סידן הידרוקסיד (Ca(OH)2)
סיד כבוי, בנייה
אשלגן הידרוקסיד (KOH)
סבון נוזלי, סוללות
סודה לשתייה (NaHCO3)
בסיס חלש, באפייה
 מנין חומצות ובסיסים? קצת היסטוריה
מנין חומצות ובסיסים? קצת היסטוריה
המילה 'חומצה' באנגלית (Acid) מגיעה מהלטינית acidus - חמוץ. כימאים במשך מאות שנים ניסו להבין מה הופך חומר לחומצי. רק בסוף המאה ה-19 הצליח המדען השבדי סבאנטה ארניוס לנסח הגדרה מדויקת.
הגדרות היסטוריות - מארניוס ועד לואיס
ארניוס (1887)
חומצה = משחררת H+ במים. בסיס = משחרר OH- במים. ההגדרה שאנו משתמשים בה בעיקר בכיתה ט'.
ברונסטד-לאורי (1923)
חומצה = תורמת פרוטון (H+). בסיס = מקבל פרוטון. הגדרה רחבה יותר - עובדת גם בלי מים.
לואיס (1938)
חומצה = מקבלת זוג אלקטרונים. בסיס = תורם זוג אלקטרונים. ההגדרה הרחבה ביותר.
 שאלה לחשיבה
שאלה לחשיבה
לפי הגדרת ארניוס, בסיס חייב לשחרר OH- במים. אבל אמוניה (NH3) נחשבת בסיס, למרות שאין בה OH-. כיצד זה ייתכן?
כשאמוניה (NH3) מומסת במים, היא מגיבה עם מולקולת מים ו'לוקחת' ממנה יון H+. כך נוצר יון אמוניום (NH4+) ונשאר יון הידרוקסיל (OH-): NH3 + H2O ← NH4+ + OH-. אמנם אין OH- במולקולה המקורית, אבל התגובה עם מים יוצרת OH-. לפי הגדרת ברונסטד-לאורי, NH3 היא בסיס כי היא מקבלת פרוטון.
 חומצות ובסיסים הם אלקטרוליטים
חומצות ובסיסים הם אלקטרוליטים
נקודת מפתח: כל חומצה ובסיס שנלמד הם אלקטרוליטים - התמיסות שלהם מוליכות חשמל. הסיבה: בתהליך הדיסוציאציה נוצרים יונים חופשיים שנושאים מטען חשמלי ומאפשרים מעבר זרם. ככל שהדיסוציאציה מלאה יותר, כך נוצרים יותר יונים והמוליכות גבוהה יותר.
ניסוי פשוט: חברו נורה למעגל חשמלי עם שני אלקטרודות. טבלו את האלקטרודות במים טהורים - הנורה לא תידלק (כמעט אין יונים). הוסיפו HCl - הנורה תידלק בעוצמה (הרבה יונים). הוסיפו חומץ - הנורה תידלק חלש (מעט יונים). ההבדל? HCl עוברת דיסוציאציה מלאה, חומץ רק חלקית.
 ניסוי מחשבה: זיהוי חומצות ובסיסים
ניסוי מחשבה: זיהוי חומצות ובסיסים
שלבי הניסוי
שלב 1: הכנה
הכינו מבחנות עם תמיסות שונות: מיץ לימון, חומץ, מים, סודה לשתייה, סבון נוזלי.
שלב 2: הוספת אינדיקטור
הוסיפו 2-3 טיפות מיצוי כרוב סגול לכל מבחנה ותעדו את שינוי הצבע.
שלב 3: תיעוד
רשמו את הצבע שהתקבל בכל מבחנה בטבלת תוצאות מסודרת.
שלב 4: מסקנות
סווגו כל תמיסה: חומצית, בסיסית או ניטרלית על פי צבע האינדיקטור.
 שאלה לחשיבה
שאלה לחשיבה
כשמוסיפים מיצוי כרוב סגול למיץ לימון, הצבע משתנה לאדום. כשמוסיפים אותו לאקונומיקה, הצבע משתנה לצהוב-ירוק. מה ניתן ללמוד על שני החומרים?
מיץ לימון הוא חומצי - אינדיקטור כרוב סגול הופך לאדום בסביבה חומצית, מה שמעיד שמיץ לימון מכיל חומצה (חומצה ציטרית, pH בערך 2). אקונומיקה היא בסיסית - האינדיקטור הופך לצהוב-ירוק בסביבה בסיסית חזקה (pH בערך 12-13). כרוב סגול הוא אינדיקטור יעיל כי הוא נותן צבעים שונים לכל טווח pH.
 שאלה לחשיבה
שאלה לחשיבה
חומצת מלח (HCl) היא חומצה חזקה, וחומצה אצטית (CH3COOH, חומץ) היא חומצה חלשה. שתיהן בריכוז זהה של 0.1 mol/L. באיזו תמיסה ריכוז יוני ההידרוניום יהיה גבוה יותר? מדוע?
ריכוז יוני ההידרוניום יהיה גבוה יותר בתמיסת חומצת המלח. הסיבה: HCl היא חומצה חזקה שעוברת דיסוציאציה מלאה - כל 0.1 mol/L של מולקולות מתפרקות ליונים, אז ריכוז H3O+ = 0.1 mol/L. לעומת זאת, חומצה אצטית עוברת דיסוציאציה חלקית - רק כ-1% מהמולקולות מתפרקות, אז ריכוז H3O+ הוא רק 0.001 mol/L בקירוב.
 בטיחות בעבודה עם חומצות ובסיסים
בטיחות בעבודה עם חומצות ובסיסים
חומצות ובסיסים חזקים עלולים לגרום לכוויות כימיות. חוקי הבטיחות:
- תמיד להרכיב משקפי מגן וכפפות
- לעולם לא לטעום חומרי מעבדה
- להוסיף חומצה למים, לא מים לחומצה (התגובה פולטת חום רב!)
- לעולם לא לערבב אקונומיקה עם חומצה - נפלטים גזים מסוכנים!
- במקרה של שפיכה על העור - לשטוף מיד בזרם מים שוטפים למשך 15 דקות
לפי הגדרת ברונסטד-לאורי, מים יכולים לתפקד גם כחומצה וגם כבסיס. חומר כזה נקרא אמפוטרי (amphoteric).
כאשר מים פוגשים חומצה חזקה, הם מקבלים פרוטון ופועלים כבסיס:
HCl + H2O ← H3O+ + Cl-
כאשר מים פוגשים בסיס חזק, הם תורמים פרוטון ופועלים כחומצה:
NH3 + H2O ← NH4+ + OH-
מים הם גם הממס הנפוץ ביותר לתגובות חומצה-בסיס. בלעדיהם, רוב התגובות שנלמד בפרק זה לא היו מתרחשות!
מייקל פאראדיי, אחד מגדולי המדענים במאה ה-19, גילה שתמיסות של חומצות ובסיסים מוליכות חשמל. הוא טבע את המונח אלקטרוליט (electrolyte) לתיאור חומרים שיוצרים יונים בתמיסה.
פאראדיי הראה שהמוליכות תלויה בכמות היונים: תמיסה מרוכזת יותר מוליכה יותר, וחומצה חזקה מוליכה יותר מחומצה חלשה באותו ריכוז. תגלית זו חיברה בין כימיה לפיזיקה ופתחה את הדרך להבנת מבנה החומר.