סולם pH
מספר אחד שמתאר כמה חומצי או בסיסי חומר - כלי מרכזי בכימיה
 מהו pH?
מהו pH?
 סולם pH - מ-0 עד 14
סולם pH - מ-0 עד 14
סולם ה-pH נע מ-0 עד 14 ומחלק את התמיסות לשלוש קבוצות.
pH < 7 = תמיסה חומצית
ככל שהמספר נמוך יותר, החומצה חזקה יותר.
ריכוז H3O+ גבוה מריכוז OH-.
pH = 7 = תמיסה ניטרלית
ריכוז H3O+ שווה לריכוז OH-.
מים טהורים בטמפרטורת החדר.
pH > 7 = תמיסה בסיסית
ככל שהמספר גבוה יותר, הבסיס חזק יותר.
ריכוז OH- גבוה מריכוז H3O+.
pH נמוך = חומצי, pH = 7 = ניטרלי, pH גבוה = בסיסי.
 סולם לוגריתמי - מה זה אומר?
סולם לוגריתמי - מה זה אומר?
 חשוב להבין
חשוב להבין
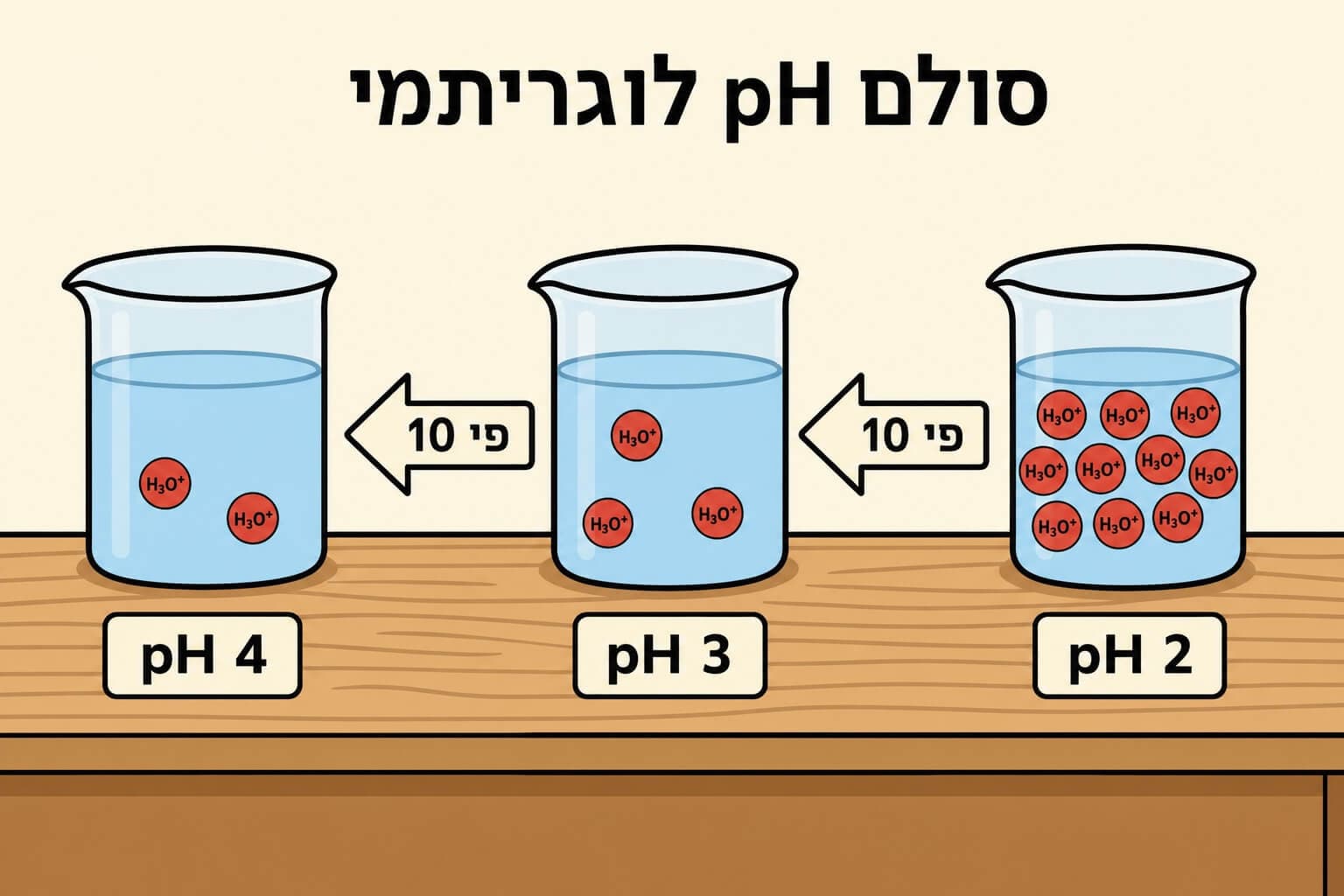
סולם pH הוא סולם לוגריתמי. המשמעות: כל הפרש של יחידת pH אחת מייצג הבדל של פי 10 בריכוז יוני ההידרוניום.
לדוגמה:
- תמיסה עם pH = 3 חומצית פי 10 מתמיסה עם pH = 4
- תמיסה עם pH = 3 חומצית פי 100 מתמיסה עם pH = 5
- תמיסה עם pH = 3 חומצית פי 1,000 מתמיסה עם pH = 6
לכן, הפרש 'קטן' ב-pH מייצג הבדל עצום בריכוז היונים.
 שאלה לחשיבה
שאלה לחשיבה
מדוע בחרו מדענים בסולם לוגריתמי ולא בסולם רגיל לתיאור חומציות?
הטווח של ריכוזי H3O+ בתמיסות הוא עצום - מ-1 mol/L (חומצה חזקה מרוכזת) עד 10^-14 mol/L (בסיס חזק מרוכז). הבדל של 100,000,000,000,000 פעמים! אם היינו משתמשים בסולם רגיל, היינו צריכים מספרים עם 14 ספרות. סולם לוגריתמי 'דוחס' את כל הטווח הזה ל-14 יחידות נוחות. המדען הדני סורן סורנסן הציע את הסולם ב-1909.
 דוגמה מספרית - הבינו את הגודל
דוגמה מספרית - הבינו את הגודל
pH = 2 (מיץ לימון)
ריכוז H3O+ = 0.01 mol/L
(10^-2)
זה אומר שבכל ליטר תמיסה יש 0.01 מול של יוני הידרוניום - כ-6 x 10^21 יונים!
pH = 7 (מים טהורים)
ריכוז H3O+ = 0.0000001 mol/L
(10^-7)
פי 100,000 פחות יונים מאשר במיץ לימון. ההבדל עצום!
pH = 12 (אקונומיקה)
ריכוז H3O+ = 10^-12 mol/L
כמעט אין יוני H3O+.
לעומת זאת, ריכוז OH- = 10^-2 = 0.01 mol/L - גבוה מאוד.
ההשוואה
בין pH 2 ל-pH 12:
ריכוז H3O+ יורד פי 10^10 = פי 10,000,000,000!
ריכוז OH- עולה באותו יחס.
 חומרים נפוצים על סולם pH
חומרים נפוצים על סולם pH
חומרים נפוצים על סולם pH
| חומר | pH בקירוב | סוג | הערה |
|---|---|---|---|
| חומצת קיבה | 1-2 | חומצי מאוד | הורגת חיידקים ומפרקת מזון |
| מיץ לימון | 2 | חומצי | חומצה ציטרית |
| חומץ | 3 | חומצי | חומצה אצטית 5% |
| מיץ תפוזים | 3.5 | חומצי | חומצה ציטרית ואסקורבית |
| גשם חומצי | 3-4 | חומצי | H2SO4 ו-HNO3 מזיהום |
| קפה שחור | 5 | חומצי חלש | חומצות אורגניות מגוונות |
| גשם רגיל | 5.6 | חומצי מעט | H2CO3 מ-CO2 טבעי |
| חלב | 6.5 | חומצי מעט | חומצה לקטית |
| מים טהורים | 7 | ניטרלי | [H3O+] = [OH-] |
| דם אנושי | 7.35-7.45 | בסיסי מעט | טווח צר, חיוני לחיים |
| סודה לשתייה | 8.5 | בסיסי | NaHCO3 |
| סבון | 10 | בסיסי | מפרק שומנים |
| אמוניה ביתית | 11 | בסיסי חזק | NH3 בתמיסה |
| אקונומיקה | 12-13 | בסיסי חזק | NaClO |
| NaOH מרוכז | 14 | בסיסי מאוד | סותר כימי חזק |
* שימו לב: דם אנושי הוא בסיסי מעט (7.4). שינוי קטן ב-pH הדם עלול לסכן חיים.
 שיטות מדידת pH
שיטות מדידת pH
 כלי מדידה - מפשוט למדויק
כלי מדידה - מפשוט למדויק
נייר pH אוניברסלי
פשוט ומהיר
רצועת נייר ספוגה בתערובת אינדיקטורים
טובלים בתמיסה ומשווים לסולם צבעים
דיוק: יחידה שלמה (לא עשרוניות)
זול ונוח לשימוש בשטח
מתאים לזיהוי מהיר ראשוני
אינדיקטור נוזלי
לניסויים
טיפות נוזל שמשנות צבע
לכל אינדיקטור טווח pH שונה
פנולפתלאין - שקוף/ורוד
לקמוס - אדום/סגול/כחול
מתאים לטיטרציה ולניסויים
חיישן pH דיגיטלי
הכי מדויק
מכשיר אלקטרוני עם אלקטרודה
מודד מתח חשמלי בתמיסה
דיוק: עד 0.01 יחידות pH
דורש כיול תקופתי
סטנדרט במעבדה מקצועית
 pH בגוף האדם - מפעל כימי מתוחכם
pH בגוף האדם - מפעל כימי מתוחכם
הגוף שלנו הוא מפעל כימי מדהים שבו כל איבר עובד ב-pH שונה. חשבו על זה: הקיבה חומצית מאוד (pH 1-2) כדי לפרק מזון ולהרוג חיידקים, אבל המעי הדק בסיסי (pH 8) כי אנזימי העיכול שם עובדים טוב דווקא בסביבה בסיסית.
pH באיברים שונים
- קיבה: pH 1-2 (חומצי מאוד - לפירוק מזון ולהרג חיידקים)
- רוק: pH 6.5-7.5 (קרוב לניטרלי - תחילת עיכול פחמימות)
- דם: pH 7.35-7.45 (טווח צר מאוד - סטייה מסכנת חיים)
- מעי דק: pH 8 (בסיסי - לפעולת אנזימי עיכול)
- שתן: pH 4.6-8 (משתנה לפי תזונה ומצב בריאותי)
- עור: pH 4.5-5.5 (חומצי - מגן מפני חיידקים)
pH הדם - שמירה קריטית על יציבות
הגוף משקיע אנרגיה רבה בשמירה על pH הדם בטווח 7.35-7.45.
ירידה מתחת ל-7.35 = חמצת (acidosis)
עלייה מעל 7.45 = בססת (alkalosis)
שני המצבים מסכנים חיים!
מנגנונים בגוף שומרים על pH יציב:
- חוצצים בדם (מערכת כימית)
- ריאות (פולטות CO2)
- כליות (מפרישות H+ או OH-)
זוהי דוגמה מצוינת להומיאוסטזיס.
 שאלה לחשיבה
שאלה לחשיבה
מה pH גבוה יותר: מיץ לימון (pH=2) או חומץ (pH=3)? איזה מהם חומצי יותר? בכמה פעמים?
pH של חומץ (3) גבוה יותר מ-pH של מיץ לימון (2). אבל מיץ לימון חומצי יותר - כי pH נמוך יותר = יותר חומצי. מכיוון שהסולם לוגריתמי, ההבדל של יחידה אחת מייצג פי 10 בריכוז. מיץ לימון חומצי פי 10 מחומץ - ריכוז יוני ההידרוניום במיץ לימון גבוה פי 10.
 שאלה לחשיבה
שאלה לחשיבה
תמיסה A בעלת pH = 4. תמיסה B בעלת pH = 1. כמה פעמים ריכוז יוני ההידרוניום בתמיסה B גבוה מאשר בתמיסה A?
ההפרש ב-pH הוא 3 יחידות (4 - 1 = 3). מכיוון שסולם pH הוא לוגריתמי, כל יחידה מייצגת הבדל של פי 10. לכן ריכוז H3O+ בתמיסה B גבוה פי 10^3 = פי 1,000 מאשר בתמיסה A.
 שאלה לחשיבה
שאלה לחשיבה
pH של בריכת שחייה צריך להיות 7.2-7.6. מנהל הבריכה מדד pH של 8.2. מה עליו לעשות, ומדוע חשוב לתקן?
pH 8.2 גבוה מדי (בסיסי מדי). צריך להוסיף חומצה (בדרך כלל חומצת מלח מדוללת) כדי להוריד את ה-pH ל-7.2-7.6. חשוב לתקן כי ב-pH גבוה מדי: (1) הכלור לא עובד כמחטא - חיידקים יכולים לשגשג, (2) המים נעשים עכורים, (3) אבנית מתגבשת על הצנרת.
במים טהורים מתרחשת תגובה עצמית (אוטופרוטוליזה):
H2O + H2O ← H3O+ + OH-
בטמפרטורת החדר (25 מעלות), ריכוז כל אחד מהיונים הוא בדיוק 10^-7 mol/L. לכן:
pH = -log(10^-7) = 7
נקודה מעניינת: בטמפרטורות גבוהות יותר, pH של מים טהורים יורד מתחת ל-7 (כי האוטופרוטוליזה מוגברת). אבל המים עדיין ניטרליים - כי ריכוז H3O+ עדיין שווה לריכוז OH-. ניטרלי לא אומר pH=7 בהכרח, אלא שהריכוזים שווים.
אמרנו שסולם pH נע בין 0 ל-14, אבל זה לא מדויק לחלוטין! חומצות מרוכזות מאוד יכולות להגיע לערכי pH שליליים.
לדוגמה, תמיסת HCl בריכוז 10 mol/L תהיה בעלת pH = -1. ובסיסים מרוכזים מאוד יכולים להגיע ל-pH > 14.
בפועל, בכיתה ט' נעבוד בטווח 0-14 שמכסה את הרוב המוחלט של התמיסות שניפגש.
לסיכום: סולם pH הוא כלי פשוט אך עוצמתי שמאפשר לנו לתאר בקלות את מידת החומציות או הבסיסיות של תמיסה. זכרו: הסולם לוגריתמי - כך שהבדל קטן ב-pH מייצג הבדל גדול מאוד בריכוז היונים.