טיטרציה
הטכניקה המעבדתית שמאפשרת לנו לגלות כמה חומצה או בסיס יש בתמיסה - בדיוק מרשים
 בלשות כימית - כמה חומצה בתמיסה?
בלשות כימית - כמה חומצה בתמיסה?
 ציוד לטיטרציה
ציוד לטיטרציה
הכלים שצריך
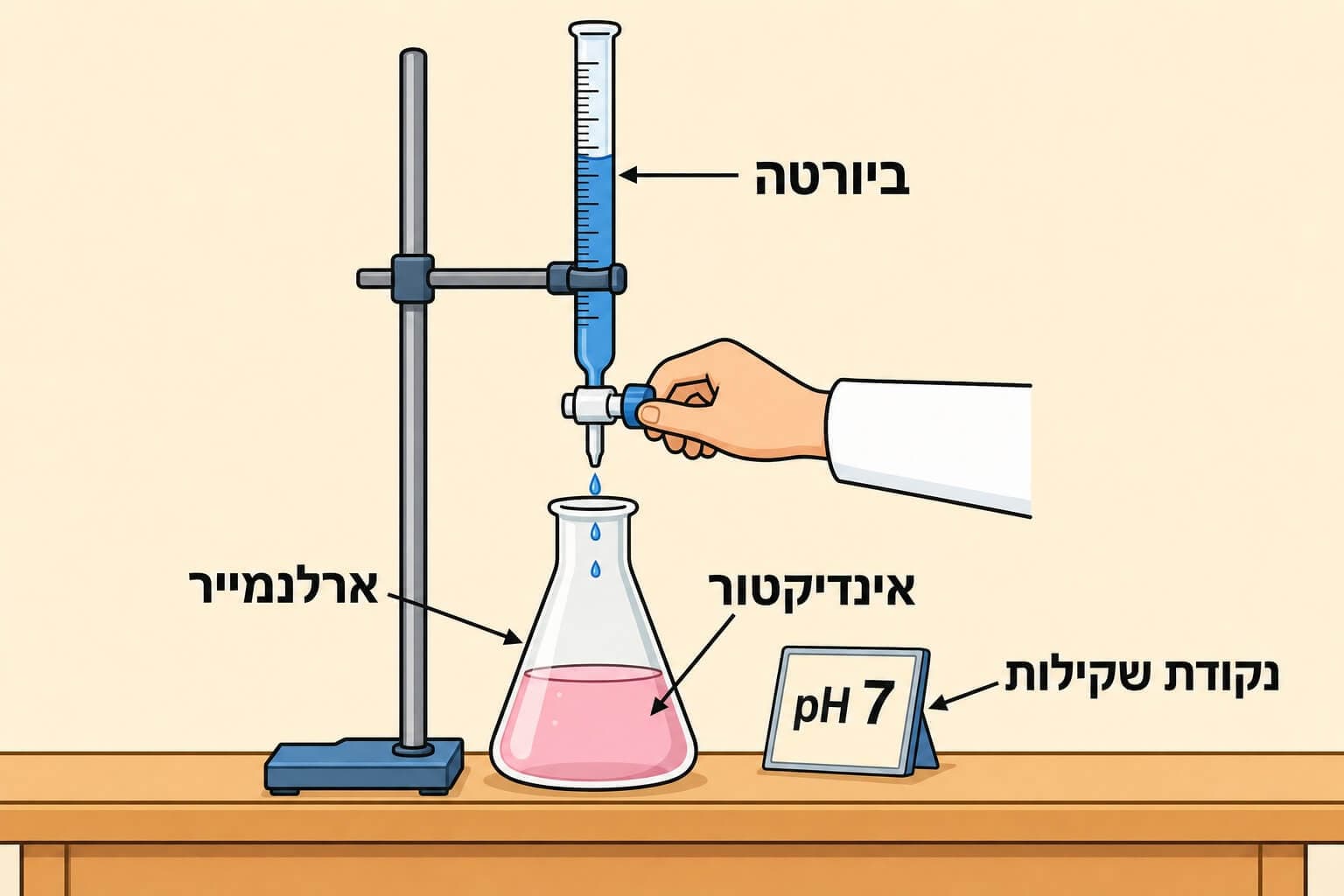
בירטה (Burette)
צינור זכוכית מדורג עם ברז בתחתית. מאפשרת לטפטף תמיסה בדיוק של 0.05 mL. כאן שמים את התמיסה הידועה.
ארלנמאייר (Erlenmeyer)
כוס חרוטית עם צוואר צר. כאן שמים את התמיסה הלא ידועה + אינדיקטור. הצורה מונעת התזות.
אינדיקטור
פנולפתלאין (הנפוץ ביותר) או מתיל כתום. מסמן את הרגע המדויק שהסתירה הושלמה.
פיפטה / צילינדר מדידה
למדידת נפח מדויק של התמיסה הלא ידועה. פיפטה מדויקת יותר מצילינדר.
תמיסת סטנדרט
תמיסה בריכוז ידוע ומדויק. בדרך כלל NaOH או HCl. מכניסים אותה לבירטה.
מגנט לערבוב
מערבב את התמיסה באופן אחיד. חשוב שהתגובה תתרחש בכל נפח הכוס.
 שלבי הטיטרציה - צעד אחר צעד
שלבי הטיטרציה - צעד אחר צעד
 תהליך הטיטרציה
תהליך הטיטרציה
נבצע טיטרציה של חומצה לא ידועה (HCl) עם בסיס ידוע (NaOH) באמצעות פנולפתלאין.
שלב 1 - הכנה:
מלאו את הבירטה בתמיסת NaOH (ריכוז ידוע, למשל 0.1 mol/L).
מדדו נפח מדויק של תמיסת HCl (למשל 25 mL) לארלנמאייר.
הוסיפו 2-3 טיפות פנולפתלאין - התמיסה שקופה (חומצית).
שלב 2 - טיפטוף:
פתחו את ברז הבירטה בזהירות וטפטפו NaOH לאט.
ערבבו בעדינות. בהתחלה, צבע ורוד נעלם מיד.
שלב 3 - התקרבות:
ככל שמתקרבים לנקודת השקילות, הצבע הורוד נעלם לאט יותר.
האטו את הטפטוף! טיפה אחת יכולה לעשות את ההבדל.
שלב 4 - נקודת השקילות:
טיפה אחת נוספת - והצבע הורוד נשאר ולא נעלם!
זו נקודת השקילות - כל החומצה נוטרלה.
רשמו את נפח NaOH שנדרש (קראו מהבירטה). עכשיו יש לכם את כל הנתונים לחישוב!
 חישוב ריכוז - המתמטיקה
חישוב ריכוז - המתמטיקה
בנקודת השקילות, מספר המולים של החומצה שווה למספר המולים של הבסיס (ביחס לפי המשוואה המאוזנת). הנוסחה הבסיסית:
מולים = ריכוז x נפח
n = C x V
כאשר:
n = מספר מולים (mol)
C = ריכוז (mol/L)
V = נפח (L) - חשוב: בליטרים! (mL / 1000)
בנקודת השקילות (עבור HCl + NaOH):
C(חומצה) x V(חומצה) = C(בסיס) x V(בסיס)
 דוגמה מספרית מפורטת
דוגמה מספרית מפורטת
חישוב ריכוז HCl
נתון: 25 mL של HCl (ריכוז לא ידוע). הוספנו NaOH בריכוז 0.1 mol/L. נקודת השקילות הושגה אחרי 20 mL של NaOH.
פתרון:
מולי NaOH = C x V = 0.1 x 0.020 = 0.002 mol
מולי HCl = 0.002 mol (יחס 1:1)
ריכוז HCl = n / V = 0.002 / 0.025 = 0.08 mol/L
תשובה: ריכוז חומצת המלח הוא 0.08 mol/L.
 שאלה לחשיבה
שאלה לחשיבה
בטיטרציה, הוספנו 30 mL של NaOH בריכוז 0.1 mol/L לכוס עם 50 mL של HCl. הגענו בדיוק לנקודת השקילות. מהו ריכוז ה-HCl?
מולי NaOH = ריכוז x נפח = 0.1 x 0.030 = 0.003 mol.
בנקודת השקילות (יחס 1:1): מולי HCl = 0.003 mol.
ריכוז HCl = מולים / נפח = 0.003 / 0.050 = 0.06 mol/L.
ריכוז חומצת המלח הוא 0.06 mol/L.
 שאלה לחשיבה
שאלה לחשיבה
בטיטרציה של H2SO4 (חומצה דו-ערכית) עם NaOH, צריך 40 mL של NaOH בריכוז 0.2 mol/L כדי לסתור 20 mL של H2SO4. מהו ריכוז החומצה?
המשוואה: H2SO4 + 2NaOH ← Na2SO4 + 2H2O. היחס הוא 1:2 (מול אחד חומצה צריך 2 מולי בסיס).
מולי NaOH = 0.2 x 0.040 = 0.008 mol.
מולי H2SO4 = 0.008 / 2 = 0.004 mol (חילקנו ב-2 בגלל היחס).
ריכוז H2SO4 = 0.004 / 0.020 = 0.2 mol/L.
 נקודת השקילות - הרגע המכריע
נקודת השקילות - הרגע המכריע
נקודת השקילות (equivalence point) היא הרגע שבו כמות יוני H3O+ מהחומצה שווה בדיוק לכמות יוני OH- מהבסיס. ברגע זה, כל החומצה נוטרלה (או כל הבסיס נוטרל).
 האם נקודת השקילות תמיד ב-pH 7?
האם נקודת השקילות תמיד ב-pH 7?
לא! רק בסתירה של חומצה חזקה + בסיס חזק. בשאר המקרים:
חומצה חזקה + בסיס חזק: pH = 7 (ניטרלי)
חומצה חלשה + בסיס חזק: pH > 7 (בסיסי מעט) - כי המלח עובר הידרוליזה
חומצה חזקה + בסיס חלש: pH < 7 (חומצי מעט)
לכן בחירת האינדיקטור חשובה - הוא צריך לשנות צבע בקרבת נקודת השקילות האמיתית.
 שימושים מעשיים של טיטרציה
שימושים מעשיים של טיטרציה
בדיקת איכות מזון
בדיקת אחוז החומצה בחומץ (צריך להיות לפחות 4-5%).
בדיקת חומציות חלב - חלב חמוץ מכיל יותר חומצה לקטית.
בדיקת ויטמין C בפירות.
כל מפעל מזון מבצע טיטרציות שגרתיות לבקרת איכות.
איכות הסביבה
בדיקת חומציות מי גשם - מעקב אחר גשם חומצי.
בדיקת pH מי שתייה.
ניטור שפכים תעשייתיים.
בדיקת חומציות קרקע לחקלאות.
טיטרציה היא כלי מרכזי בניטור סביבתי.
 שאלה לחשיבה
שאלה לחשיבה
מדוע חשוב לטפטף את הבסיס לאט מאוד כשמתקרבים לנקודת השקילות? מה יקרה אם נוסיף יותר מדי?
כשמתקרבים לנקודת השקילות, נשארה רק כמות קטנה של חומצה שלא נוטרלה. טיפה אחת של בסיס יכולה לגרום לקפיצה גדולה ב-pH. אם נוסיף יותר מדי, נעבור את נקודת השקילות - יהיה עודף בסיס ולא נוכל לחשב את הריכוז בדיוק. במקרה כזה, צריך להתחיל את הניסוי מחדש! לכן מתרגלים טיפטוף איטי ומדויק.
 טיפים להצלחה בטיטרציה
טיפים להצלחה בטיטרציה
טיטרציה מדויקת דורשת סבלנות וטכניקה:
- קראו את נפח ההתחלה בבירטה לפני שמתחילים
- בהתחלה אפשר לטפטף מהר, אבל כשהצבע מתחיל להישאר - האטו!
- ערבבו בעדינות אחרי כל טיפה
- הצבע צריך להישאר לפחות 30 שניות כדי שנדע שזו נקודת השקילות
- חזרו על הניסוי 3 פעמים וחשבו ממוצע - כך מקבלים תוצאה אמינה יותר
- המירו mL ל-L לפני חישוב! (חלקו ב-1000)
אם נמדוד pH אחרי כל תוספת של בסיס ונשרטט גרף, נקבל עקומת טיטרציה (titration curve). הגרף מראה:
- בהתחלה: pH נמוך (חומצי), עולה לאט
- לפני נקודת השקילות: pH עולה מהר מאוד (קפיצה חדה)
- בנקודת השקילות: pH בקירוב 7 (חומצה חזקה + בסיס חזק)
- אחרי נקודת השקילות: pH ממשיך לעלות לאט
הנקודה שבה הגרף הכי תלול היא בדיוק נקודת השקילות. בנקודה זו, תוספת של טיפה אחת גורמת לקפיצה הגדולה ביותר ב-pH.
מכשיר pH דיגיטלי מאפשר לשרטט עקומה כזו בדיוק רב. בתיכון ובאוניברסיטה תלמדו לנתח עקומות טיטרציה מורכבות.
בתעשיית התרופות, טיטרציה היא שלב קריטי בבקרת איכות. כל אצווה של תרופה נבדקת בטיטרציה כדי לוודא שהריכוז מדויק. טעות קטנה יכולה להפוך תרופה מועילה למסוכנת.
בתעשיית המזון, טיטרציה קובעת את אחוז החומצה בחומץ, את רמת הוויטמין C במיצים, ואת טריות החלב. חלב שהחומציות שלו עלתה מעבר לסף מסוים נפסל לשימוש.
טיטרציות אוטומטיות (עם רובוטים) מבצעות מאות בדיקות ביום במפעלים מודרניים.