סיכום - חומצות, בסיסים וסולם pH
חזרה מקיפה על כל מה שלמדנו בפרק ההרחבה
 מה למדנו בפרק זה?
מה למדנו בפרק זה?
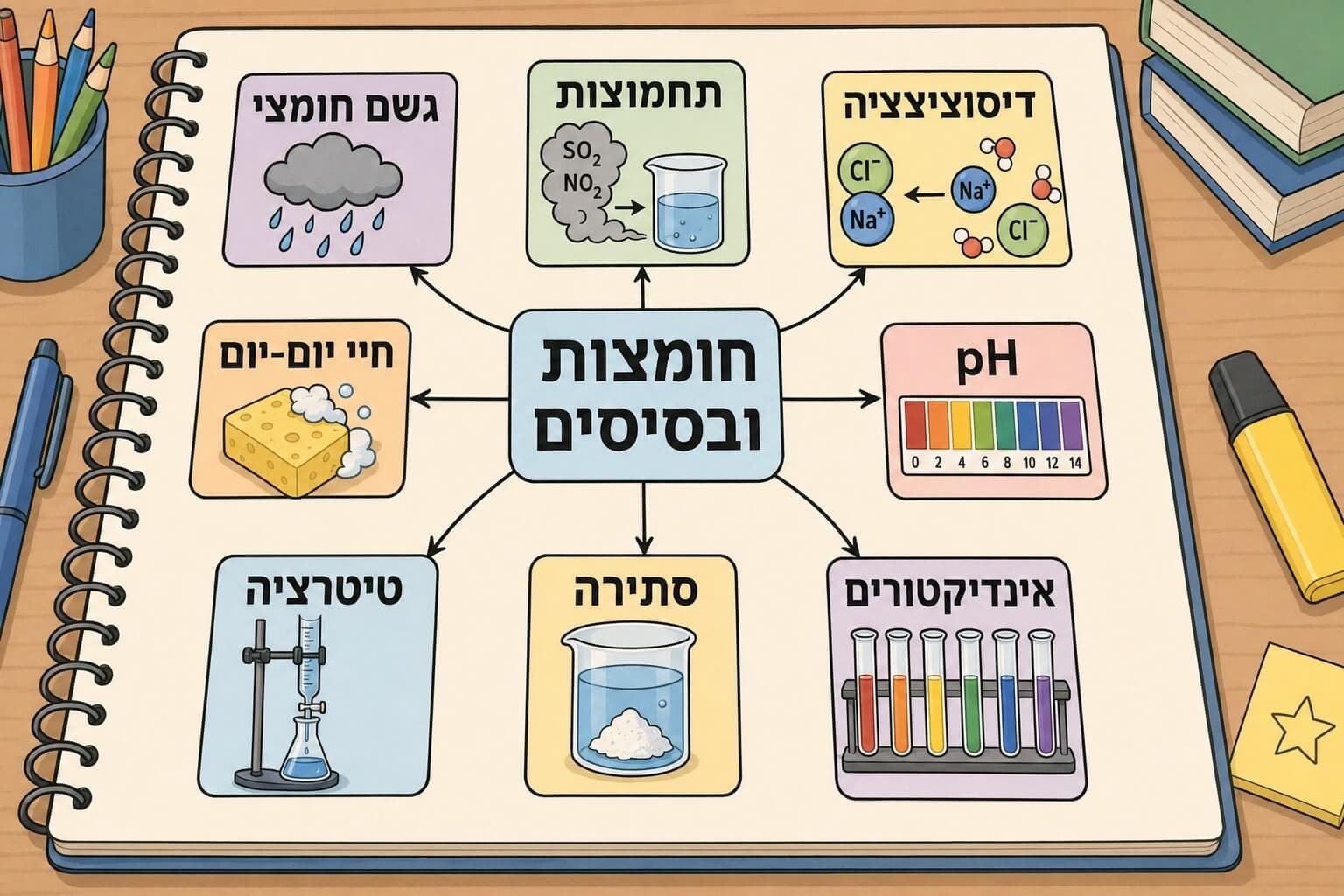
 חומצות מול בסיסים - סיכום
חומצות מול בסיסים - סיכום
 חומצות מול בסיסים
חומצות מול בסיסים
 חומצות
חומצות
טעם חמוץ
משחררות H3O+ (הידרוניום)
pH < 7
מגיבות עם מתכות (שחרור H2)
לקמוס ← אדום
מוליכות חשמל בתמיסה
חזקות: דיסוציאציה מלאה (HCl, H2SO4, HNO3)
חלשות: דיסוציאציה חלקית (CH3COOH, H2CO3)
דוגמה: נוצרות מתחמוצות אל-מתכות + מים
 בסיסים
בסיסים
מרגישים חלקלקים, טעם מריר
משחררים OH- (הידרוקסיל)
pH > 7
מפרקים שומנים
לקמוס ← כחול
מוליכים חשמל בתמיסה
חזקים: דיסוציאציה מלאה (NaOH, KOH, Ca(OH)2)
חלשים: דיסוציאציה חלקית (NH3, NaHCO3)
דוגמה: נוצרים מתחמוצות מתכות + מים
 תחמוצות - סיכום
תחמוצות - סיכום
כלל זהב:
תחמוצת אל-מתכת + H2O ← חומצה
SO3 + H2O ← H2SO4
CO2 + H2O ← H2CO3
NO2 + H2O ← HNO3
תחמוצת מתכת + H2O ← בסיס
MgO + H2O ← Mg(OH)2
CaO + H2O ← Ca(OH)2
Na2O + H2O ← 2NaOH
 דיסוציאציה - חזק מול חלש
דיסוציאציה - חזק מול חלש
חזק מול חלש - השוואה
| תכונה | חזק | חלש |
|---|---|---|
| דיסוציאציה | מלאה (100%) | חלקית (1-5%) |
| תגובה | בלתי הפיכה (←) | הפיכה (⇌) |
| יונים בתמיסה | הרבה | מעט |
| מוליכות חשמלית | גבוהה | נמוכה |
| דוגמאות חומצות | HCl, H2SO4, HNO3 | CH3COOH, H2CO3 |
| דוגמאות בסיסים | NaOH, KOH, Ca(OH)2 | NH3, NaHCO3 |
* עוצמה (חזק/חלש) היא תכונה קבועה. ריכוז (מרוכז/מדולל) ניתן לשינוי - אלו שני מושגים שונים!
 סולם pH - סיכום
סולם pH - סיכום
סולם pH - חלוקה
| טווח pH | סוג | יון שולט | דוגמאות |
|---|---|---|---|
| 0-2 | חומצי מאוד | H3O+ בריכוז גבוה מאוד | חומצת קיבה, HCl מרוכז |
| 3-4 | חומצי | H3O+ בריכוז גבוה | מיץ לימון, חומץ, גשם חומצי |
| 5-6 | חומצי חלש | H3O+ בריכוז נמוך | קפה, חלב, גשם רגיל |
| 7 | ניטרלי | H3O+ = OH- | מים טהורים |
| 8-9 | בסיסי חלש | OH- בריכוז נמוך | סודה לשתייה, דם (7.4) |
| 10-11 | בסיסי | OH- בריכוז גבוה | סבון, אמוניה |
| 12-14 | בסיסי מאוד | OH- בריכוז גבוה מאוד | אקונומיקה, NaOH |
* הסולם לוגריתמי: כל יחידת pH = פי 10 בריכוז יוני הידרוניום
 אינדיקטורים - סיכום
אינדיקטורים - סיכום
אינדיקטורים נפוצים
| אינדיקטור | בחומצה | ניטרלי | בבסיס | שימוש עיקרי |
|---|---|---|---|---|
| לקמוס | אדום | סגול | כחול | זיהוי מהיר |
| פנולפתלאין | שקוף | שקוף | ורוד | טיטרציה |
| מתיל כתום | אדום | כתום | צהוב | טיטרציה חומצית |
| כרוב סגול | אדום/ורוד | סגול | ירוק/צהוב | ניסויים, כל הטווח |
| נייר pH | אדום-כתום | ירוק | כחול-סגול | מדידת pH |
 תגובת סתירה וטיטרציה - סיכום
תגובת סתירה וטיטרציה - סיכום
תגובת סתירה:
חומצה + בסיס ← מלח + מים
H3O+ + OH- ← 2H2O
טיטרציה:
הוספה הדרגתית של בסיס (ידוע) לחומצה (לא ידועה) עד נקודת השקילות.
נקודת שקילות = כמות H3O+ שווה לכמות OH-.
חישוב: C(חומצה) x V(חומצה) = C(בסיס) x V(בסיס) (ביחס 1:1)
מאפיינים:
- pH מתקרב ל-7 (חזק+חזק) או סביב 7 (חלש+חזק)
- תגובה פולטת חום (אקסותרמית)
- נוצר מלח (תרכובת יונית)
 גשם חומצי - סיכום
גשם חומצי - סיכום
גורמים
שריפת דלקים מאובנים
← SO2 + NOx לאוויר
← תגובה עם אדי מים
← H2SO4 + HNO3 (חזקות!)
← גשם עם pH < 5
תחמוצת אל-מתכת + מים = חומצה
נזקים
פגיעה בצמחים ויערות
הרס מקורות מים - דגים מתים
שחיקת מבנים ופסלים (CaCO3)
האצת חלודה
פגיעה בבריאות (עקיפה)
פתרונות
מניעה: אנרגיות מתחדשות
סינון פליטות (Scrubbers)
ממירים קטליטיים ברכבים
טיפול: סיוד אגמים/קרקעות
חקיקה סביבתית (עובדת!)
 נוסחאות ותגובות חשובות
נוסחאות ותגובות חשובות
כל התגובות הכימיות מהפרק
| תגובה | משוואה | סוג |
|---|---|---|
| סתירה בסיסית | HCl + NaOH ← NaCl + H2O | סתירה |
| סתירה חומצה דו-ערכית | H2SO4 + 2NaOH ← Na2SO4 + 2H2O | סתירה |
| תחמוצת אל-מתכת + מים | SO3 + H2O ← H2SO4 | חומצה מתחמוצת |
| תחמוצת מתכת + מים | MgO + H2O ← Mg(OH)2 | בסיס מתחמוצת |
| תחמוצת מתכת + מים | CaO + H2O ← Ca(OH)2 | בסיס מתחמוצת |
| גשם חומצי | 2NO2 + H2O ← HNO3 + HNO2 | חומצה מתחמוצת |
| גשם רגיל | CO2 + H2O ← H2CO3 | חומצה פחמתית |
| סיוד | CaCO3 + H2SO4 ← CaSO4 + H2O + CO2 | סתירה |
| ניקוי אבנית | CaCO3 + 2HCl ← CaCl2 + H2O + CO2 | סתירה |
| דיסוציאציה מלאה | HCl ← H+ + Cl- | חומצה חזקה |
| דיסוציאציה חלקית | CH3COOH ⇌ H+ + CH3COO- | חומצה חלשה |
 מושגי מפתח
מושגי מפתח
מושגים בסיסיים
- חומצה - חומר שמשחרר H3O+ במים
- בסיס - חומר שמשחרר OH- במים
- אינדיקטור - חומר שמשנה צבע לפי pH
- דיסוציאציה - התפרקות ליונים במים
- pH - מדד חומציות/בסיסיות (0-14)
- ניטרלי - pH = 7, ריכוז יונים שווה
- תחמוצת - תרכובת יסוד עם חמצן
מושגים מתקדמים
- תגובת סתירה - חומצה + בסיס ← מלח + מים
- טיטרציה - מדידת ריכוז בסתירה מבוקרת
- נקודת שקילות - ניטרול מלא
- סולם לוגריתמי - כל יחידה = פי 10
- ריכוז מול עוצמה - מושגים שונים!
- גשם חומצי - pH < 5 מזיהום
- סיוד - ניטרול חומציות בסביבה
 טיפים למבחן
טיפים למבחן
נקודות חשובות לזכור:
- pH נמוך = חומצי, pH גבוה = בסיסי, pH = 7 = ניטרלי
- הסולם לוגריתמי - יחידה אחת = פי 10 בריכוז
- חזק = דיסוציאציה מלאה, חלש = דיסוציאציה חלקית (אל תבלבלו עם ריכוז!)
- תחמוצת אל-מתכת + מים = חומצה, תחמוצת מתכת + מים = בסיס
- תגובת סתירה תמיד מייצרת מלח + מים, פולטת חום
- בטיטרציה: C x V (חומצה) = C x V (בסיס) ביחס לפי המשוואה
- גשם רגיל pH = 5.6 (CO2 טבעי), גשם חומצי pH < 5 (זיהום SO2, NOx)
- סיוד = הוספת בסיס (CaCO3) לנטרל חומציות - תגובת סתירה
מה מבדיל בין חומצה לבסיס ברמה היונית?
תרגול מתקדם
מוכנים למבחן המסכם המלא?
עברו לחידון המורחב של הפרק לתרגול מקיף עם 130 שאלות מכל נושאי הלימוד.