תחמוצות, חומצות ובסיסים
מנין באות חומצות ובסיסים? הסוד בתחמוצות - תוצרי בעירה שפוגשות מים
 תחמוצות - חומרים שנולדים מחמצון
תחמוצות - חומרים שנולדים מחמצון
 מה זו תחמוצת?
מה זו תחמוצת?
תחמוצת (oxide) היא תרכובת של יסוד כלשהו עם חמצן (O2). כשיסוד נשרף באוויר או מגיב עם חמצן, נוצרת תחמוצת. הנוסחה הכללית היא: יסוד + O2 ← תחמוצת.
השאלה המרכזית היא: מה קורה כשתחמוצת פוגשת מים? התשובה תלויה בשאלה האם מדובר בתחמוצת של אל-מתכת או של מתכת.
 תחמוצות אל-מתכות ← חומצות
תחמוצות אל-מתכות ← חומצות
 תחמוצת אל-מתכת + מים = חומצה
תחמוצת אל-מתכת + מים = חומצה
כשאל-מתכת (כמו גופרית, חנקן, פחמן) נשרפת ותחמוצת שלה מגיבה עם מים - נוצרת חומצה.
דוגמה 1: גופרית
שלב 1: S + O2 ← SO2 (גופרית נשרפת)
שלב 2: 2SO2 + O2 ← 2SO3 (חמצון נוסף)
שלב 3: SO3 + H2O ← H2SO4 (חומצה גופרתית)
דוגמה 2: חנקן
בטמפרטורות גבוהות (מנוע): N2 + O2 ← 2NO
באוויר: 2NO + O2 ← 2NO2
במים: 3NO2 + H2O ← 2HNO3 + NO (חומצה חנקתית)
דוגמה 3: פחמן
C + O2 ← CO2
CO2 + H2O ← H2CO3 (חומצה פחמתית - חלשה)
תחמוצות אל-מתכות הן 'חומצות בכוח' - כשהן פוגשות מים, הן הופכות לחומצות. ככל שהאל-מתכת פעילה יותר, החומצה שנוצרת חזקה יותר.
תחמוצות אל-מתכות והחומצות שנוצרות מהן
| אל-מתכת | תחמוצת | חומצה שנוצרת | עוצמה | מקור בטבע |
|---|---|---|---|---|
| גופרית (S) | SO3 | H2SO4 (חומצה גופרתית) | חזקה מאוד | שריפת פחם, הרי געש |
| גופרית (S) | SO2 | H2SO3 (חומצה גופריתית) | חלשה | שריפת פחם |
| חנקן (N) | NO2 | HNO3 (חומצה חנקתית) | חזקה | מנועי רכב, ברקים |
| פחמן (C) | CO2 | H2CO3 (חומצה פחמתית) | חלשה | נשימה, בעירה, משקאות מוגזים |
| זרחן (P) | P2O5 | H3PO4 (חומצה זרחתית) | בינונית | תעשיית דשנים |
* שימו לב: CO2 מפיק חומצה חלשה בלבד. לכן גשם רגיל (pH 5.6) אינו מזיק. SO2 ו-NO2 מפיקים חומצות חזקות - הם גורמי הגשם החומצי.
 שאלה לחשיבה
שאלה לחשיבה
כשאתם פותחים בקבוק של משקה מוגז ושומעים 'פשש', מה קורה מבחינה כימית? למה המשקה חמצמץ?
בבקבוק סגור, CO2 מומס תחת לחץ. כשפותחים, הלחץ יורד ו-CO2 מתחיל להשתחרר כבועות. חלק מה-CO2 שנשאר מגיב עם המים: CO2 + H2O ← H2CO3 (חומצה פחמתית). חומצה פחמתית היא חומצה חלשה שנותנת את הטעם החמצמץ. ככל שהמשקה 'מתאוורר', יותר CO2 בורח ופחות חומצה נשארת - לכן משקה מוגז שעמד פתוח מאבד את הטעם.
 תחמוצות מתכות ← בסיסים
תחמוצות מתכות ← בסיסים
 תחמוצת מתכת + מים = בסיס
תחמוצת מתכת + מים = בסיס
כשמתכת פעילה (כמו נתרן, מגנזיום, סידן) נשרפת ותחמוצת שלה מגיבה עם מים - נוצר בסיס.
דוגמה 1: מגנזיום
שלב 1: 2Mg + O2 ← 2MgO (מגנזיום נשרף באור בוהק!)
שלב 2: MgO + H2O ← Mg(OH)2 (מגנזיום הידרוקסיד)
דוגמה 2: נתרן
שלב 1: 4Na + O2 ← 2Na2O
שלב 2: Na2O + H2O ← 2NaOH (נתרן הידרוקסיד - בסיס חזק!)
דוגמה 3: סידן
שלב 1: 2Ca + O2 ← 2CaO (סיד חי)
שלב 2: CaO + H2O ← Ca(OH)2 (סיד כבוי)
תחמוצות מתכות הן 'בסיסים בכוח' - כשהן פוגשות מים, הן הופכות לבסיסים. ככל שהמתכת פעילה יותר, הבסיס שנוצר חזק יותר.
תחמוצות מתכות והבסיסים שנוצרים מהן
| מתכת | תחמוצת | בסיס שנוצר | עוצמה | שימוש |
|---|---|---|---|---|
| נתרן (Na) | Na2O | NaOH (נתרן הידרוקסיד) | חזק מאוד | ייצור סבון, תעשייה |
| אשלגן (K) | K2O | KOH (אשלגן הידרוקסיד) | חזק מאוד | סבון נוזלי, סוללות |
| סידן (Ca) | CaO | Ca(OH)2 (סידן הידרוקסיד) | חזק | בנייה, סיוד קרקע |
| מגנזיום (Mg) | MgO | Mg(OH)2 (מגנזיום הידרוקסיד) | חלש | נוגד חומצה (תרופה) |
* CaO (סיד חי) מגיב בחוזקה עם מים ופולט חום רב - לכן הוא 'חי'. Ca(OH)2 (סיד כבוי) כבר הגיב ולכן 'כבוי'.
 שאלה לחשיבה
שאלה לחשיבה
בבניין ישן, הטיח (סיד כבוי - Ca(OH)2) 'מתקשה' עם הזמן. כתבו את התגובה הכימית שגורמת לכך, בידיעה שיש CO2 באוויר.
Ca(OH)2 (סיד כבוי, בסיס) מגיב עם CO2 (שנוצרת ממנו חומצה פחמתית) מהאוויר: Ca(OH)2 + CO2 ← CaCO3 + H2O. נוצר סידן פחמתי (CaCO3) שהוא מוצק קשה - זה אבן הגיר! בעצם, הטיח 'חוזר' להיות אבן. תהליך זה לוקח שבועות וזו הסיבה שטיח רטוב צריך זמן ל'התייבשות' (שהיא בעצם תגובה כימית).
 הכלל הגדול - תמונה שלמה
הכלל הגדול - תמונה שלמה
 תחמוצות אל-מתכות מול תחמוצות מתכות
תחמוצות אל-מתכות מול תחמוצות מתכות
 תחמוצת אל-מתכת
תחמוצת אל-מתכת
נוצרת מבעירת אל-מתכת (S, N, C, P)
מגיבה עם מים ← חומצה
דוגמאות:
SO3 + H2O ← H2SO4
CO2 + H2O ← H2CO3
רלוונטיות: גשם חומצי
זיהום אוויר מתעשייה ותחבורה
דוגמה: תחמוצת אל-מתכת + H2O ← חומצה
 תחמוצת מתכת
תחמוצת מתכת
נוצרת מבעירת מתכת (Na, Mg, Ca, K)
מגיבה עם מים ← בסיס
דוגמאות:
MgO + H2O ← Mg(OH)2
CaO + H2O ← Ca(OH)2
רלוונטיות: בנייה, תעשייה
ייצור סבון, סיוד קרקעות
דוגמה: תחמוצת מתכת + H2O ← בסיס
כלל זהב: אל-מתכת + O2 ← תחמוצת חומצית | מתכת + O2 ← תחמוצת בסיסית
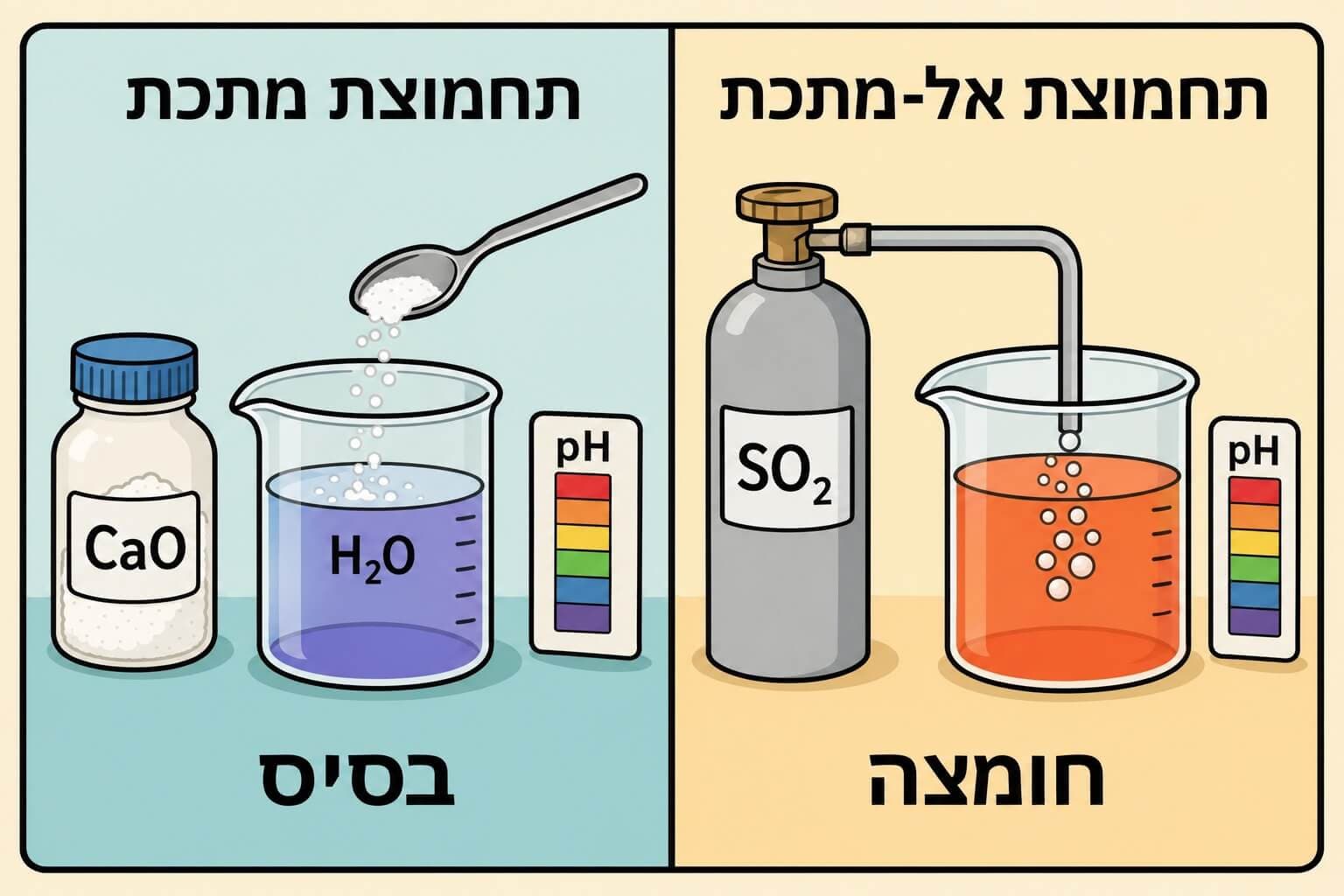
 הקשר לגשם חומצי
הקשר לגשם חומצי
עכשיו אתם מבינים בדיוק איך נוצר גשם חומצי! כששורפים דלקים מאובנים (פחם, נפט), הגופרית והחנקן שבהם נשרפים גם כן ויוצרים תחמוצות אל-מתכות: SO2, NO2. התחמוצות האלה עולות לאטמוספירה, מגיבות עם מי גשם, ויוצרות חומצות חזקות: H2SO4 ו-HNO3. נלמד על כך לעומק בשיעור על גשם חומצי.
 שאלה לחשיבה
שאלה לחשיבה
הר געש מתפרץ ופולט SO2 לאטמוספירה. כמה ימים אחר כך, גשם עם pH = 3.5 יורד במרחק 200 קילומטר מההר. הסבירו את הקשר.
SO2 (תחמוצת אל-מתכת) שנפלט מההר הגעשי עלה לאטמוספירה ונישא ברוח 200 ק"מ. באטמוספירה, SO2 עבר חמצון נוסף: 2SO2 + O2 ← 2SO3. ואז SO3 הגיב עם אדי מים: SO3 + H2O ← H2SO4 (חומצה גופרתית, חומצה חזקה). כשהגשם ירד, הוא הכיל חומצה גופרתית וה-pH ירד ל-3.5 - גשם חומצי. זו דוגמה לגשם חומצי ממקור טבעי, לא רק מזיהום תעשייתי.
סיד חי (CaO) הוא חומר מרתק. כשמוסיפים לו מים, מתרחשת תגובה אקסותרמית (פולטת חום) כל כך עזה שהמים יכולים להרתיח!
CaO + H2O ← Ca(OH)2 + חום רב
בעבר, חיילים רומאים השתמשו בסיד חי לחימום אוכל בשדה הקרב - הם שמו CaO בכלי עם מים ותוך דקות המים רתחו! גם היום יש ערכות חימום עצמי למזון צבאי שפועלות על אותו עיקרון.
בתעשיית הבנייה, הוספת מים לסיד חי ('כיבוי סיד') היא תהליך מסוכן - יש ללבוש ציוד מגן כי החום הרב והאדים הבסיסיים עלולים לגרום לכוויות.
יש תחמוצות שלא מתנהגות בבירור כחומצה או כבסיס - הן אמפוטריות. דוגמה חשובה: אלומיניום תחמוצת (Al2O3).
Al2O3 יכולה להגיב עם חומצה (מתנהגת כבסיס) או עם בסיס (מתנהגת כחומצה). זו הסיבה שאלומיניום נמצא 'באמצע' הטבלה המחזורית - הוא לא מתכת טיפוסית ולא אל-מתכת.
יסודות נוספים עם תחמוצות אמפוטריות: אבץ (ZnO), בדיל (SnO), עופרת (PbO).
לסיכום: תחמוצות הן ה'גשר' בין בעירה לבין חומצות ובסיסים. תחמוצות אל-מתכות + מים = חומצות. תחמוצות מתכות + מים = בסיסים. כלל זה מסביר תופעות טבעיות (גשם חומצי, קרקע בסיסית) ותהליכים תעשייתיים (ייצור חומצות, בנייה).