גשם חומצי
כשזיהום אוויר הופך גשם למזיק - הקשר בין תעשייה, כימיה וסביבה
 גשם שהורס במקום להשקות
גשם שהורס במקום להשקות
 איך נוצר גשם חומצי?
איך נוצר גשם חומצי?
 תהליך היווצרות גשם חומצי
תהליך היווצרות גשם חומצי
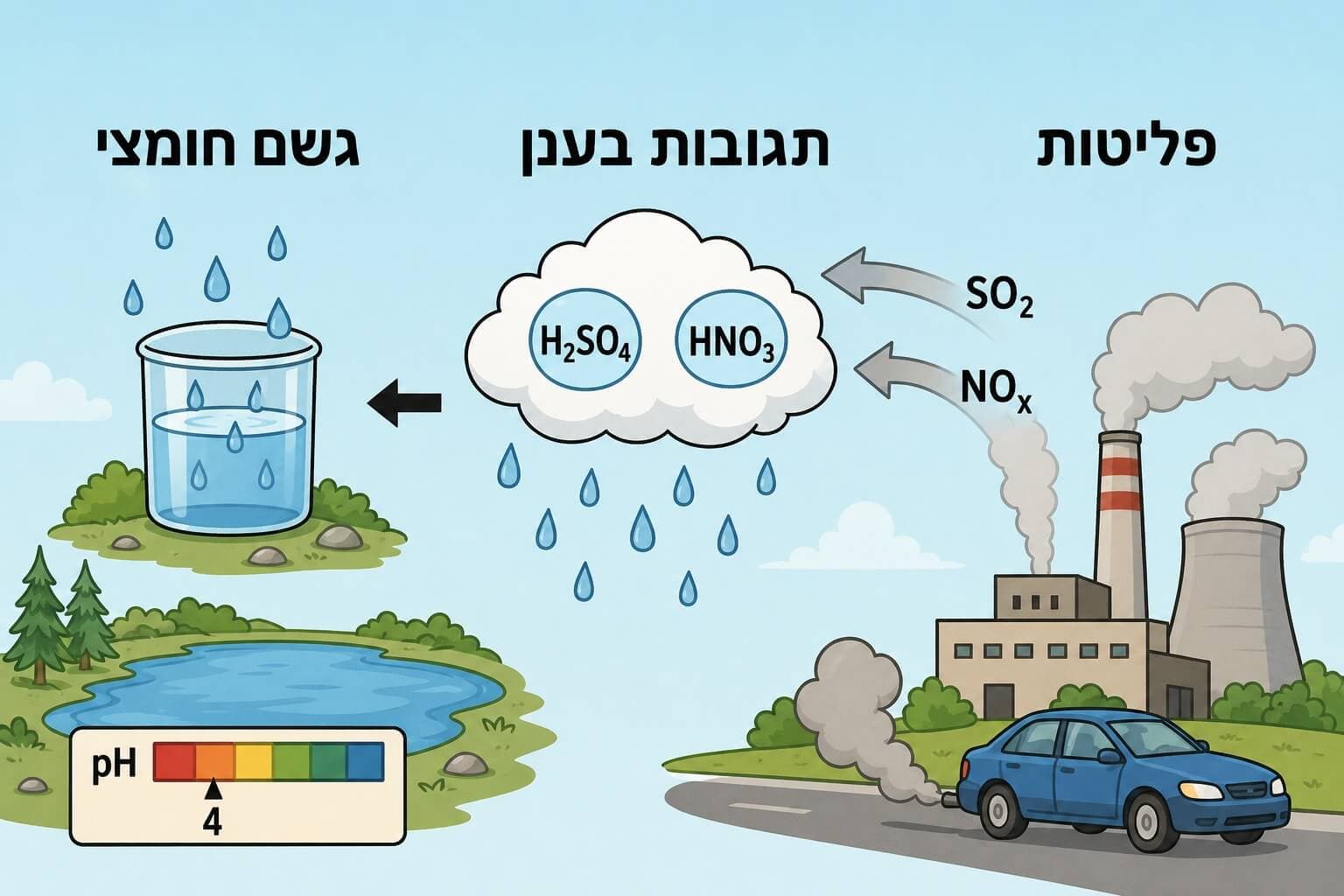
גשם חומצי נוצר כאשר תחמוצות של גופרית וחנקן מגיבות עם מי גשם ויוצרות חומצות חזקות.
שלב 1 - פליטה:
שריפת דלקים מאובנים (פחם, נפט, גז) בתחנות כוח, מפעלים ורכבים:
- תחמוצות גופרית (SO2, SO3)
- תחמוצות חנקן (NO, NO2 - ביחד NOx)
שלב 2 - תגובה באטמוספירה:
SO2 + H2O ← H2SO3 (חומצה גופריתית)
SO3 + H2O ← H2SO4 (חומצה גופרתית - חזקה!)
2NO2 + H2O ← HNO3 + HNO2 (חומצות חנקן)
שלב 3 - הגשם:
החומצות מומסות בטיפות הגשם ויורדות לקרקע.
גשם רגיל: pH 5.6 (CO2 טבעי ← H2CO3 חלשה)
גשם חומצי: pH < 5 (לפעמים pH 3-4!)
זיהום אוויר ← תחמוצות ← חומצות באטמוספירה ← גשם חומצי. הקשר לשיעור על תחמוצות ברור!
 מדוע גשם רגיל הוא בעל pH 5.6?
מדוע גשם רגיל הוא בעל pH 5.6?
גם ללא זיהום, גשם טבעי הוא קצת חומצי. הסיבה: CO2 שקיים באוויר באופן טבעי (כ-0.04%) מגיב עם אדי מים:
CO2 + H2O ← H2CO3 (חומצה פחמתית - חלשה)
חומצה זו מורידה את pH הגשם מ-7 ל-5.6. זו תופעה טבעית ולא מזיקה. רק כשזיהום מוסיף SO2 ו-NOx ויוצר חומצות חזקות (H2SO4, HNO3), ה-pH יורד מתחת ל-5 - ואז מדברים על גשם חומצי.
 השפעות גשם חומצי
השפעות גשם חומצי
נזקים סביבתיים - תמונה קשה
נזק לצמחים ויערות
החומצה שוטפת מינרלים חיוניים (Ca, Mg, K) מהקרקע. משחררת מתכות רעילות (אלומיניום) שמזיקות לשורשים. עלים נפגעים ונושרים. יערות שלמים יכולים למות.
נזק למקורות מים
מוריד pH אגמים ונהרות. דגים מתים כשה-pH יורד מתחת ל-5. אמפיביות (צפרדעים, סלמנדרות) רגישות במיוחד. שרשרת המזון המימית קורסת.
שחיקת מבנים ופסלים
CaCO3 (שיש, אבן גיר) + H2SO4 ← CaSO4 + H2O + CO2. מבנים היסטוריים נשחקים. פסלים מאבדים פרטים. מתכות מחלידות מהר יותר.
בריאות האדם
גשם חומצי עצמו לא מסוכן במישרין. אבל חלקיקים חומציים באוויר מחמירים אסתמה ומחלות ריאה. מתכות רעילות שמשתחררות מהקרקע חודרות למי שתייה.
 דוגמאות מהעולם - מקרים אמיתיים
דוגמאות מהעולם - מקרים אמיתיים
 מקרים ידועים של נזקי גשם חומצי
מקרים ידועים של נזקי גשם חומצי
יערות השחורים, גרמניה
בשנות ה-80, כ-50% מעצי האשוח נפגעו. עלים הצהיבו ונשרו, ועצים מתו. הסיבה: פליטות SO2 ממפעלים. היום, אחרי חקיקה, היערות מתאוששים.
אגמים בסקנדינביה
אלפי אגמים בשבדיה ונורווגיה איבדו את הדגים. הזיהום הגיע ממפעלים בבריטניה ובגרמניה - הרוח נשאה אותו מאות קילומטרים!
הטאג' מהאל, הודו
פסל השיש המפורסם נפגע מגשם חומצי. השיש הלבן הצהיב ונשחק. הממשלה הקימה אזור נקי מזיהום סביב האתר.
סין - האתגר הנוכחי
סין היא היום המדינה עם הגשם החומצי הקשה ביותר. שליש משטחה נפגע. השילוב של תעשייה מאסיבית ושימוש בפחם יוצר pH 3 ומטה.
 שאלה לחשיבה
שאלה לחשיבה
מדוע גשם חומצי יכול לפגוע באזור שרחוק 1,000 קילומטר ממקור הזיהום?
גזי SO2 ו-NOx נפלטים לגובה ונישאים ברוח מאות ואף אלפי קילומטרים. הם יכולים להישאר באטמוספירה ימים ושבועות לפני שהם מגיבים עם מים ויורדים כגשם. לכן זיהום ממפעלים במדינה אחת יכול לגרום לגשם חומצי במדינה אחרת. דוגמה: מפעלים בבריטניה גרמו לגשם חומצי בסקנדינביה. זו בעיה בינלאומית שדורשת שיתוף פעולה בין מדינות.
 פתרונות ומניעה
פתרונות ומניעה
מניעה - צמצום פליטות (הפתרון האמיתי)
- אנרגיות מתחדשות (שמש, רוח) - אין שריפת דלקים
- סינון גזי פליטה (Scrubbers) בארובות מפעלים - מסירים SO2
- ממירים קטליטיים ברכבים - הופכים NOx ל-N2 לא מזיק
- רכבים חשמליים - אפס פליטות מקומיות
- חקיקה - חוקים שמגבילים פליטות
טיפול - ניטרול נזקים (זמני)
- סיוד אגמים - הוספת CaCO3 (בסיסי) לנטרל חומציות
- סיוד קרקעות - החזרת pH לערכים תקינים
- ציפוי מבנים בחומרים עמידים לחומצה
- שיקום יערות - נטיעת עצים עמידים יותר
- ניטור - מעקב מתמשך אחר pH
 סיוד - תגובת סתירה בקנה מידה ענק
סיוד - תגובת סתירה בקנה מידה ענק
סיוד הוא יישום מעשי של תגובת סתירה לטיפול בנזקי גשם חומצי.
כשאגם הופך חומצי, מפזרים בו סידן פחמתי (CaCO3) - אבקה בסיסית.
התגובה:
CaCO3 + H2SO4 ← CaSO4 + H2O + CO2
הבסיס סותר את החומצה, ו-pH האגם עולה לערכים בטוחים.
בשבדיה לבדה, מפזרים עשרות אלפי טונות של CaCO3 מדי שנה באגמים!
אבל זהו טיפול סימפטומטי: הוא לא פותר את מקור הבעיה. צריך גם למנוע את הזיהום.
סיוד מציל אגמים, אבל המניעה האמיתית היא צמצום זיהום האוויר.
 שאלה לחשיבה
שאלה לחשיבה
פסל שיש היסטורי נשחק מגשם חומצי. כתבו את התגובה הכימית שגורמת לכך, והסבירו מדוע זו תגובת סתירה.
שיש מורכב מ-CaCO3 (סידן פחמתי) - חומר בסיסי. הגשם החומצי מכיל H2SO4 (חומצה גופרתית). התגובה: CaCO3 + H2SO4 ← CaSO4 + H2O + CO2. זו תגובת סתירה כי חומר בסיסי (CaCO3) מגיב עם חומצה (H2SO4) ויוצר מלח (CaSO4 - גבס) ומים. CO2 הוא גז שמתפזר, ו-CaSO4 מתמוסס ונשטף - כך השיש נשחק בהדרגה.
 שאלה לחשיבה
שאלה לחשיבה
מדוע גשם חומצי (pH 3) מסוכן הרבה יותר מגשם רגיל (pH 5.6) - הרי ההבדל הוא 'רק' 2.6 יחידות?
כי סולם pH הוא לוגריתמי! הבדל של 2.6 יחידות אומר שגשם חומצי חומצי פי 10^2.6 = פי 400 (!) מגשם רגיל. ריכוז יוני ההידרוניום בגשם חומצי גבוה פי 400 מגשם רגיל. זה לא 'הבדל קטן' - זה הבדל עצום. חלודה, שחיקת אבן ומוות של דגים מתרחשים בריכוזי חומצה גבוהים כאלה.
 שאלה לחשיבה
שאלה לחשיבה
ממירים קטליטיים ברכבים הפחיתו את פליטות NOx בעשרות אחוזים. כיצד הם עובדים? איזו תגובה כימית מתרחשת?
ממירים קטליטיים מכילים מתכות מזרזות (פלטינה, רודיום, פלדיום) שמאיצות תגובות כימיות ללא שהן עצמן נצרכות. התגובה המרכזית: 2NO + 2CO ← N2 + 2CO2. תחמוצות חנקן (NO) מומרות לחנקן (N2) שהוא גז בלתי מזיק (78% מהאוויר הוא N2). בנוסף: 2CO + O2 ← 2CO2 (הפחמן חד-חמצני הרעיל הופך ל-CO2). הממיר לא מסיר CO2 (גז חממה) אבל מונע פליטת NOx ו-CO.
בשנת 1990, ארצות הברית העבירה תיקון לחוק האוויר הנקי שחייב מפעלים להפחית פליטות SO2 ב-50%.
התוצאות היו מרשימות:
- פליטות SO2 ירדו ב-90% עד שנת 2020
- pH של גשם באזורים רבים עלה בחזרה
- אגמים שהיו 'מתים' החלו להתאושש - דגים חזרו!
- יערות שנפגעו מתחדשים
- העלות הכלכלית של הצמצום היתה נמוכה בהרבה מהצפי
זוהי הוכחה חזקה שחקיקה סביבתית עובדת. כשיש רצון מדיני ומדעי, אפשר לפתור בעיות סביבתיות. ישראל גם כן מפחיתה פליטות - למשל, תחנות כוח עוברות מפחם לגז טבעי (פחות SO2).
הטבע מנסה 'לתקן' את עצמו. סלעי אבן גיר (CaCO3) בקרקע פועלים כחוצץ טבעי - הם מגיבים עם גשם חומצי וממתנים את ההשפעה:
CaCO3 + H2SO4 ← CaSO4 + H2O + CO2
לכן אזורים עם קרקע גירנית (כמו חלקים מישראל) מוגנים יותר מגשם חומצי. אזורים עם קרקע גרניט (כמו סקנדינביה) פגיעים הרבה יותר - אין להם חוצץ טבעי.
זו דוגמה מרתקת לכך שגיאולוגיה וכימיה משפיעות זו על זו!
לסיכום: גשם חומצי הוא דוגמה מובהקת לקשר בין כימיה, תעשייה וסביבה. תחמוצות אל-מתכות (SO2, NOx) מזיהום אוויר מגיבות עם מים ויוצרות חומצות חזקות. הפתרון: מניעת פליטות (אנרגיות מתחדשות, סינון, חקיקה) + טיפול בנזקים (סיוד). ההצלחות מראות שאפשר!