חזק מול חלש - דיסוציאציה
מדוע HCl 'חזקה' יותר מחומץ? הכל בגלל התפרקות ליונים
 לא כל החומצות שוות
לא כל החומצות שוות
 מה זו דיסוציאציה?
מה זו דיסוציאציה?
דיסוציאציה (Dissociation) היא תהליך שבו מולקולה מתפרקת ליונים כשהיא נכנסת למים. כל חומצה ובסיס עוברים דיסוציאציה - זה מה שהופך אותם לחומציים או בסיסיים. השאלה היא: כמה מהמולקולות מתפרקות?
 חומצות חזקות - דיסוציאציה מלאה
חומצות חזקות - דיסוציאציה מלאה
 מהי חומצה חזקה?
מהי חומצה חזקה?
חומצה חזקה היא חומצה שעוברת דיסוציאציה מלאה במים - 100% מהמולקולות מתפרקות ליונים.
נניח ששמנו 100 מולקולות של HCl (חומצת מלח) במים.
בחומצה חזקה: כל 100 המולקולות מתפרקות!
HCl ← H+ + Cl- (100% דיסוציאציה)
התוצאה: 100 יוני H+ (שהופכים ל-H3O+) ו-100 יוני Cl-.
לא נשארת אף מולקולת HCl שלמה בתמיסה.
ריכוז H3O+ = ריכוז ההתחלתי של החומצה.
לכן: חומצה חזקה ← הרבה יוני H3O+ ← pH נמוך מאוד.
בחומצה חזקה, כל מולקולה 'תורמת' יון הידרוניום. זו דיסוציאציה מלאה ובלתי הפיכה.
 שלוש החומצות החזקות שחובה לדעת
שלוש החומצות החזקות שחובה לדעת
HCl - חומצת מלח
HCl ← H+ + Cl-
100% דיסוציאציה
נמצאת בקיבה שלנו!
pH של קיבה: 1-2
שימושים: תעשייה, ניקוי מתכות
H2SO4 - חומצה גופרתית
H2SO4 ← 2H+ + SO4^2-
100% דיסוציאציה
משחררת 2 יוני H+!
(חומצה דו-ערכית)
מצברי מכוניות, דשנים
HNO3 - חומצה חנקתית
HNO3 ← H+ + NO3-
100% דיסוציאציה
ייצור דשנים וחומרי נפץ
חומצה מחמצנת חזקה
 חומצות חלשות - דיסוציאציה חלקית
חומצות חלשות - דיסוציאציה חלקית
 מהי חומצה חלשה?
מהי חומצה חלשה?
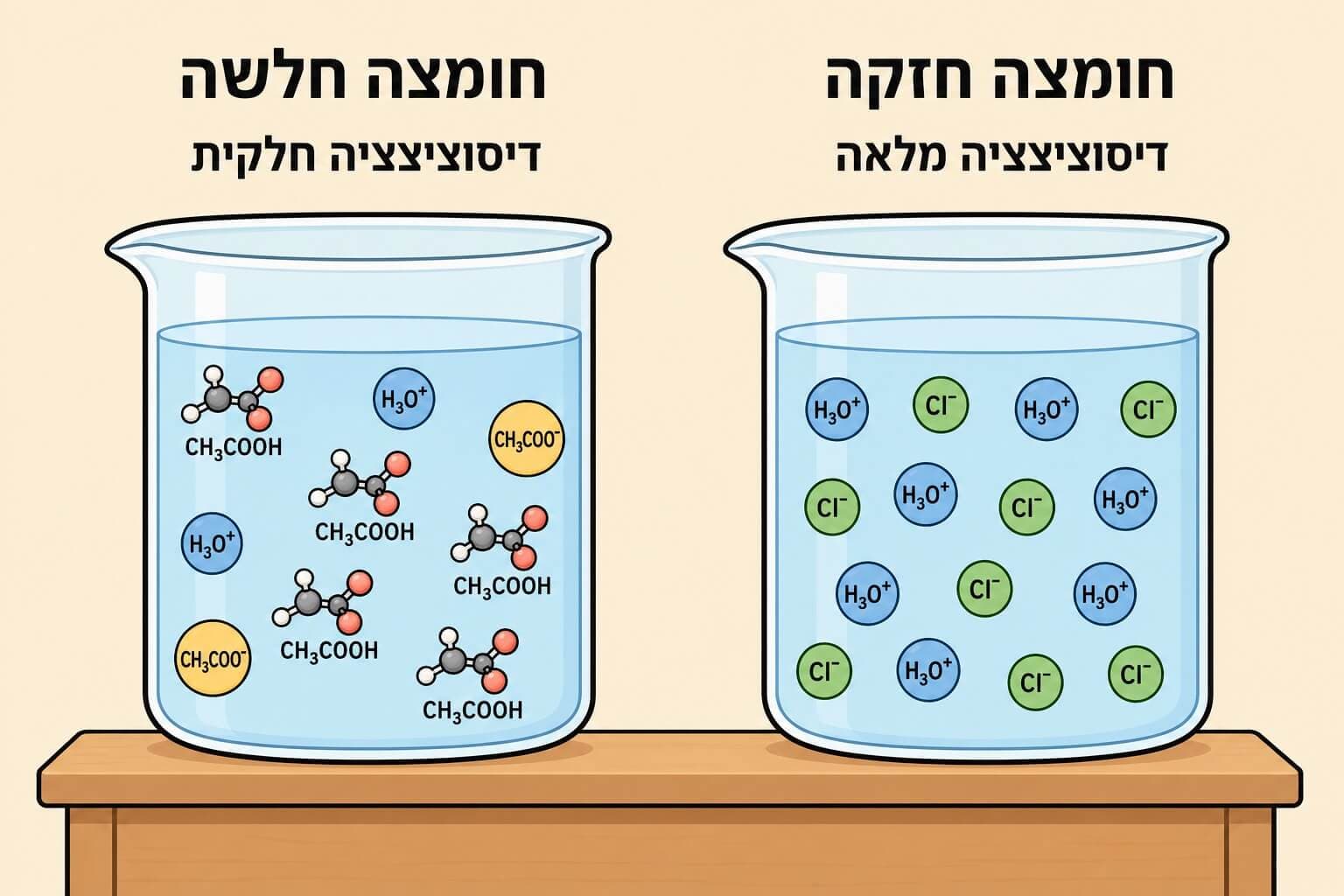
חומצה חלשה היא חומצה שעוברת דיסוציאציה חלקית - רק אחוז קטן מהמולקולות מתפרק ליונים.
נניח ששמנו 100 מולקולות של CH3COOH (חומצה אצטית, חומץ) במים.
בחומצה חלשה: רק כ-1-5 מולקולות מתפרקות!
CH3COOH ⇌ H+ + CH3COO- (רק ~1% דיסוציאציה)
התוצאה: רק 1-5 יוני H3O+, ו-95-99 מולקולות CH3COOH נשארות שלמות.
שימו לב לחץ הכפול (⇌) - התגובה הפיכה! חלק מהיונים מתחברים בחזרה למולקולות.
נוצר שיווי משקל בין מולקולות שלמות ליונים.
בחומצה חלשה, רוב המולקולות נשארות שלמות. לכן ריכוז H3O+ נמוך יותר ו-pH גבוה יותר מחומצה חזקה באותו ריכוז.
 חומצות חלשות נפוצות
חומצות חלשות נפוצות
CH3COOH - חומצה אצטית
חומץ - רכיב מוכר מהמטבח
~1% דיסוציאציה
pH של חומץ: כ-3
בטוחה יחסית למגע (מדוללת)
H2CO3 - חומצה פחמתית
נוצרת מ-CO2 + מים
חומצה חלשה מאוד
nותנת טעם למשקאות מוגזים
גורמת ל-pH 5.6 של גשם רגיל
חומצה ציטרית
בלימון, תפוז, אשכולית
נותנת טעם חמוץ
משמשת כמשמר מזון
חומצה טבעית ובטוחה
חומצה אסקורבית
ויטמין C
חיונית למערכת החיסון
חומצה חלשה מאוד
מונעת צפדינה
 בסיסים חזקים וחלשים
בסיסים חזקים וחלשים
אותו עיקרון בדיוק חל על בסיסים: בסיס חזק עובר דיסוציאציה מלאה ומשחרר הרבה יוני OH-. בסיס חלש עובר דיסוציאציה חלקית ומשחרר מעט יוני OH-.
 בסיסים חזקים מול בסיסים חלשים
בסיסים חזקים מול בסיסים חלשים
 בסיסים חזקים
בסיסים חזקים
דיסוציאציה מלאה - 100%
NaOH ← Na+ + OH-
KOH ← K+ + OH-
Ca(OH)2 ← Ca2+ + 2OH-
מסוכנים! גורמים לכוויות.
pH גבוה מאוד (12-14).
שימושים: תעשייה, ניקוי חזק.
דוגמה: NaOH, KOH, Ca(OH)2
 בסיסים חלשים
בסיסים חלשים
דיסוציאציה חלקית
NH3 + H2O ⇌ NH4+ + OH-
NaHCO3 ← Na+ + HCO3-
(HCO3- בסיסי חלש)
פחות מסוכנים.
pH בינוני (8-10).
שימושים: ניקוי, אפייה.
דוגמה: NH3, NaHCO3
שימו לב: אמוניה (NH3) היא בסיס חלש כי רק חלק קטן מהמולקולות מגיב עם מים ליצירת OH-
 ריכוז מול עוצמה - הטעות הנפוצה ביותר!
ריכוז מול עוצמה - הטעות הנפוצה ביותר!
 אל תבלבלו בין ריכוז לעוצמה!
אל תבלבלו בין ריכוז לעוצמה!
זו הטעות הנפוצה ביותר בנושא חומצות ובסיסים:
- עוצמה (חזק/חלש) = מידת הדיסוציאציה. זה תכונה של החומר עצמו ולא משתנה
- ריכוז (מרוכז/מדולל) = כמה חומר מומס בנפח מסוים. אפשר לשנות על ידי הוספת מים
- חומצה חלשה מרוכזת יכולה להיות מסוכנת יותר מחומצה חזקה מדוללת!
- דוגמה: חומץ מרוכז (20% חומצה אצטית) שורף את העור, אבל HCl מדולל מאוד (0.001%) בקושי מורגש
- במבחן: שאלות על ריכוז מול עוצמה חוזרות שוב ושוב. היו מוכנים!
 שאלה לחשיבה
שאלה לחשיבה
יש לנו שתי תמיסות: (א) חומצה אצטית (חלשה) בריכוז 1 mol/L, (ב) חומצת מלח (חזקה) בריכוז 0.001 mol/L. באיזו תמיסה ה-pH נמוך יותר?
צריך לחשב: (א) חומצה אצטית 1 mol/L, דיסוציאציה ~1%, אז ריכוז H3O+ = כ-0.004 mol/L, pH בערך 2.4. (ב) חומצת מלח 0.001 mol/L, דיסוציאציה 100%, אז ריכוז H3O+ = 0.001 mol/L, pH = 3. לכן pH של החומצה האצטית (2.4) נמוך יותר - היא חומצית יותר! למרות שחומצה אצטית 'חלשה' וחומצת מלח 'חזקה', הריכוז הגבוה של החומצה האצטית פיצה על הדיסוציאציה החלקית.
 שאלה לחשיבה
שאלה לחשיבה
שתי תמיסות באותו ריכוז (0.1 mol/L): HCl ו-CH3COOH. השוו: (א) ריכוז H3O+ (ב) pH (ג) מוליכות חשמלית.
(א) ריכוז H3O+: ב-HCl ריכוז H3O+ = 0.1 mol/L (דיסוציאציה מלאה). ב-CH3COOH ריכוז H3O+ בערך 0.001 mol/L (דיסוציאציה ~1%). HCl מכילה פי 100 יותר יוני הידרוניום. (ב) pH: HCl - pH = 1. CH3COOH - pH בערך 3. (ג) מוליכות חשמלית: HCl מוליכה הרבה יותר, כי יש בה הרבה יותר יונים חופשיים (כל המולקולות מתפרקות). CH3COOH מוליכה חלש יותר.
 סיכום ויזואלי
סיכום ויזואלי
השוואה מלאה - חזק מול חלש
| תכונה | חומצה/בסיס חזק | חומצה/בסיס חלש |
|---|---|---|
| דיסוציאציה | מלאה (100%) | חלקית (1-5%) |
| תגובה | בלתי הפיכה (←) | הפיכה (⇌) |
| יונים בתמיסה | הרבה | מעט |
| pH (לחומצה 0.1M) | 1 | כ-3 |
| מוליכות חשמלית | גבוהה | נמוכה |
| דוגמאות חומצות | HCl, H2SO4, HNO3 | CH3COOH, H2CO3, חומצה ציטרית |
| דוגמאות בסיסים | NaOH, KOH, Ca(OH)2 | NH3, NaHCO3 |
* עוצמה (חזק/חלש) היא תכונה קבועה של החומר. ריכוז (מרוכז/מדולל) ניתן לשינוי.
 שאלה לחשיבה
שאלה לחשיבה
חומצה חזקה מדוללת מאוד יכולה להיות בטוחה לשימוש, אבל חומצה חלשה מרוכזת מאוד יכולה להיות מסוכנת. תנו דוגמה מחיי היום-יום לכל מקרה.
חומצה חזקה מדוללת: חומצת מלח (HCl) בקיבה שלנו - מרוכזת מאוד (pH 1-2), אבל הקיבה מוגנת ברירית מיוחדת. HCl מאוד מדוללת (כמו במי ברז עם טיפה) לא תורגש כלל. חומצה חלשה מרוכזת: חומץ קרח (glacial acetic acid, 100% חומצה אצטית) - חומצה חלשה, אבל במצב מרוכז היא שורפת את העור ומסוכנת מאוד! חומץ רגיל הוא רק 5% חומצה אצטית ולכן בטוח יחסית.
בחומצה חלשה, התגובה הפיכה - יש שיווי משקל בין מולקולות שלמות ליונים:
CH3COOH + H2O ⇌ H3O+ + CH3COO-
בשיווי משקל, קצב ההתפרקות (קדימה) שווה לקצב ההתחברות מחדש (אחורה). זה אומר שבכל רגע נתון, יש תערובת של מולקולות שלמות ויונים. היחס ביניהם נקבע על ידי קבוע שנקרא Ka (קבוע דיסוציאציה).
ככל ש-Ka גדול יותר, כך יותר מולקולות מתפרקות והחומצה 'חזקה' יותר (בקרב החומצות החלשות). נושא זה נלמד לעומק בכימיה בתיכון.
חומצה גופרתית (H2SO4) היא חומצה דו-ערכית - היא יכולה לשחרר שני יוני H+:
שלב 1: H2SO4 ← H+ + HSO4- (דיסוציאציה מלאה)
שלב 2: HSO4- ⇌ H+ + SO4^2- (דיסוציאציה חלקית)
השלב הראשון הוא דיסוציאציה מלאה (חומצה חזקה). השלב השני הוא דיסוציאציה חלקית (HSO4- מתנהג כחומצה חלשה). לכן H2SO4 משחררת יותר יוני H3O+ מחומצה חד-ערכית באותו ריכוז, ויש צורך בכפול בסיס כדי לסתור אותה: H2SO4 + 2NaOH ← Na2SO4 + 2H2O.
לסיכום: עוצמה (חזק/חלש) מתארת את מידת הדיסוציאציה - תכונה קבועה של החומר. ריכוז (מרוכז/מדולל) מתאר כמה חומר יש בתמיסה - ניתן לשינוי. שני המושגים יחד קובעים את pH התמיסה ואת מידת הסכנה שלה.